
Date Posted
Welcome to ULACNet Update, where we share programmatic and research updates for the US-Latin American-Caribbean HIV/HPV-Cancer Prevention Clinical Trials Network (ULACNet)!
On this page
- Living with HIV and Preventing Cervical Cancer: Launch of a Transformative Study – ULACNet 202
- AQuIP Analysis: Assessing Patient Enrollment in ULACNet Screening Studies
- Screening for and Prevention of Anal Cancer as Standard of Care for People with HIV: The New Guidelines
- Auditing The ULACNet Program: One Aspect of Quality Assurance
Living with HIV and Preventing Cervical Cancer: Launch of a Transformative Study – ULACNet 202
By: Alejandra Portillo-Romero, M.D., Sc.D., Betania Allen-Leigh, Ph.D., Eduardo Lazcano-Ponce, M.D., Sc.D., Instituto Nacional de Salud Pública (INSP)
Recruiting women living with HIV (WLHIV) for research projects focused on cervical cancer prevention is a crucial and multifaceted task that requires a strategic and sensitive approach. WLHIV face a significantly higher risk of developing cervical cancer due to the increased prevalence of persistent human papillomavirus (HPV) infections. These infections, if not detected and treated in a timely manner, can progress to high-grade squamous intraepithelial lesions (HSIL) and eventually invasive cervical cancer. The study called “Optimization of Cervical Cancer Screening among Women Living with HIV in Latin American Countries” aims to develop a high-risk HPV test and a point-of-care molecular test that optimizes specificity for detecting HSIL (CIN2+) in WLHIV while maintaining high test sensitivity.
Enrolling WLHIV in research studies presents numerous challenges, including the stigma associated with HIV, insufficient information, limited acceptance and participation from healthcare providers, as well as logistical and financial obstacles (Figure 1).
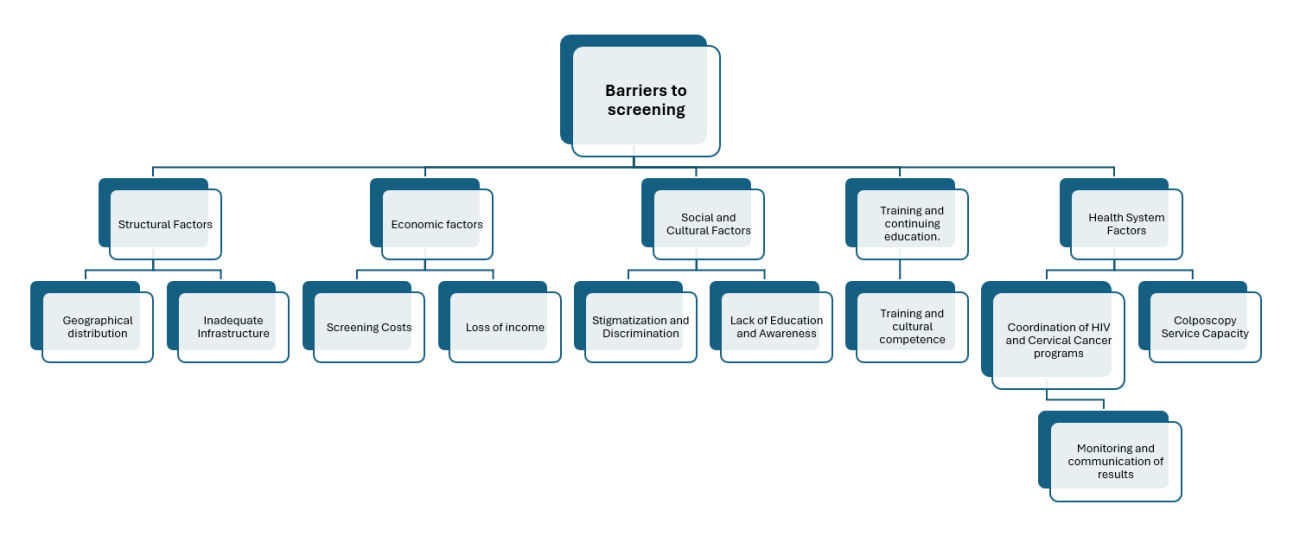
Figure 1. Barriers to HPV screening [ 1 ]

Conference "Eradication of Cervical Cancer: The Case of Mexico', by Dr. Eduardo Lazcano
It is essential to implement recruitment strategies that address these barriers. At the Mexico site within ROCCHHA, we have addressed selected barriers as follows:
1. Collaboration and Integration with the HIV Clinic (CAPASITS Puebla) and Women's Hospital of Puebla Staff
We involve both managerial and operational staff at the Clinic and Hospital to facilitate study implementation in the dysplasia unit at the Women's Hospital. We organized a presentation of the project at the Hospital, highlighting its importance, objectives, and benefits for WLHIV. During the presentation, Dr. Eduardo Lazcano delivered a keynote lecture on "Eradication of Cervical Cancer: The Case of Mexico," attended by directors, hospital physicians, gynecology residents, medical students, and INSP team members.
2. Education and Awareness for Women Attending the HIV Clinic
The physicians at the HIV clinic make an effort to provide their patients living with HIV with clear and accessible information about the benefits of cervical screening, seizing every opportunity during medical consultations, vaccination appointments, delivery of antiretroviral therapy (ART), and clinical laboratory visits. Additionally, a trained nurse conducts informational sessions for clinic healthcare users, explaining the relationship between HPV and cervical cancer, aiming to promote active participation in preventive health programs and encourage involvement in the study.

Dysplasias area where colposcopies are performed. Women's Hospital, Puebla, Mexico
3. Adequacy of Spaces and Supply of Medical Supplies
The limited capacity of health systems in middle- and lower-income countries can lead to delays in the diagnosis and treatment of precancerous lesions. We aim to optimize the dysplasia care process to prevent participants in our study from undergoing complex administrative processes to obtain a colposcopy and ensuring they receive treatment within a short time frame, thereby minimizing loss to follow-up. Additionally, we provide the Women’s Hospital of Puebla with necessary medical supplies (which are often lacking) for offering higher quality medical care, allowing the colposcopists to attend to a greater number of women (not limited to study participants).
4. Mitigating Stigma and Fear of Discrimination Among Participants
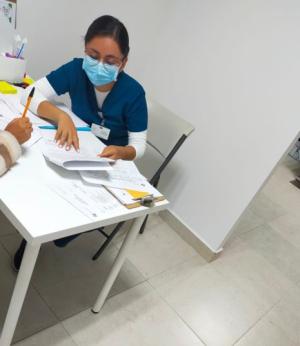
Katia Cruz-González (Site Coordinator) conducted the informed consent process, thoroughly explaining to the participants the confidentiality measures surrounding their data
Ensuring the confidentiality of participants' data and adopting a sensitive and respectful approach to their needs and concerns is essential. Therefore, the staff at the HIV clinic, the Women's Hospital of Puebla, and the INSP are continually trained on treating people living with HIV with dignity and respect. The goal is to prevent women from feeling judged or mistreated, thereby ensuring they do not miss the opportunity for timely detection and treatment if necessary. Once women are enrolled in the study, they receive clear and precise information about the protection of their personal data, and the staff maintains constant communication until they receive their results.
5. Continuous Training and Education for Healthcare Professionals
At the INSP, we are always committed to the continuous education of healthcare professionals. Through collaboration with the Women's Hospital of Puebla, we aim to engage gynecology residents as well as more experienced gynecologists and colposcopists in training and research, encouraging improvements in screening practices and the treatment of precancerous lesions. For example, in July 2024 our team members will teach an on-line course on public health research for gynecology residents at the Women’s Hospital of Puebla.
Finally, participating in this trial not only benefits the participants by providing access to preventive interventions and continuous medical monitoring, but also generates valuable knowledge that can influence public health policies and enhance cervical cancer prevention programs in our country, Mexico.
AQuIP Analysis: Assessing Patient Enrollment in ULACNet Screening Studies
By: Amina Chtourou, M.P.H.
In an effort to promote clinical trial accrual efficiency and improve study recruitment and retention, the Accrual Quality Improvement Program (AQuIP) was implemented as an accrual monitoring tool across all US-Latin American-Caribbean HIV/HPV-Cancer Prevention Clinical Trials Network (ULACNet) studies. The AQuIP program was developed by Ellen Richmond, M.S., GNP-BC in the Division of Cancer Prevention (DCP), National Cancer Institute and has been utilized in several DCP cancer prevention clinical trials networks including ULACNet over the past 10 years. AQuIP provides a platform for research staff to collect and enter participant level data through various stages of the clinical trial accrual process including the number of potential participants screened, the recruitment strategies used, the number consented, and reason(s) for not consenting or going on intervention. In addition, AQuIP employs the use of a study journal for research staff to document study-wide and site-specific events that may positively or negatively impact accrual. Examples of journal entries may include changes in the number of site staff (i.e., loss of staff or new hires), delays in receipt of study agent or supplies, weather related issues (i.e., hurricane), etc. As a result, AQuIP allows for the identification of possible barriers to participant recruitment and the potential for protocol modifications to enable more timely completion of target enrollment numbers.
AQuIP data are submitted to DCP on a monthly basis. We analyzed AQuIP data for three ULACNet screening studies (ULACNet-101, ULACNet-202, and ULACNet-302), from the beginning of patient enrollment in November 2021 through May 2024, to understand how various studies have implemented the use of AQuIP, assess participant accrual across ULACNet studies, and assess the applicability of AQuIP in clinical trials outside U.S. settings.
To date, across the three screening studies, 1,988 individuals have signed consent and 1,965 have started the study intervention, as shown in Table 1.
| Study number | Number signed consent | Number started study intervention | Target Enrollment | Study status |
|---|---|---|---|---|
| ULACNet-101 | 1,107 | 1,106 | 1,500 | ongoing |
| ULACNet-202 | 252 | 251 | 1,000 | ongoing |
| ULACNet-302 | 629 | 608 | 600 | Enrollment completed |
| Total | 1,988 | 1,965 | 3,100 |
The most common recruitment strategies across all three screening studies were ‘other’ strategies, physician referrals, and referrals through staff within the institution who were non-study staff. Figure 1 below shows recruitment strategies employed across the three screening studies. For ‘reasons not consented’, study staff often reported an ‘other’ reason, an individual declined, or an individual had a prior cancer. Figure 2 below shows ‘reasons not consented’ across the three screening studies. Figure 2 is restricted to individuals who were contacted but did not consent to join the study and does not necessarily reflect reasons participants were ineligible to start the study intervention after they signed the consent form.
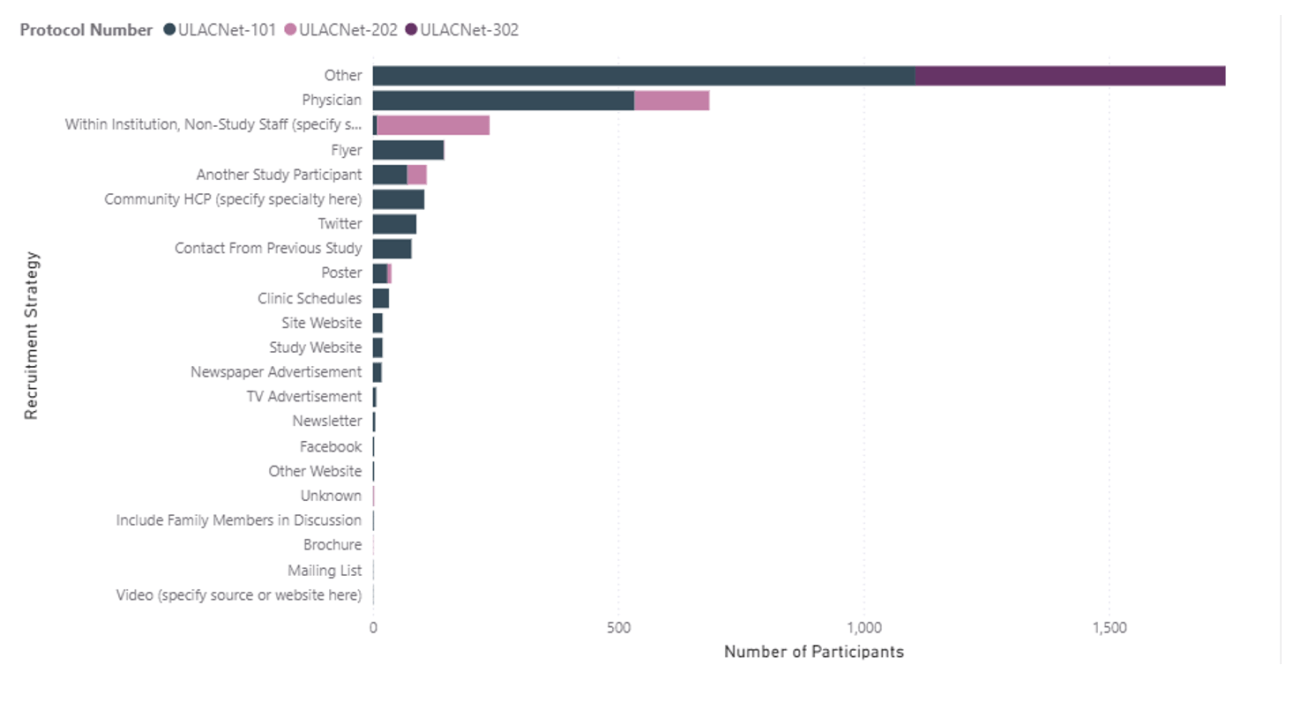
Figure 1. ULACNet Screening Studies Participant Recruitment Strategies [ 2 ]
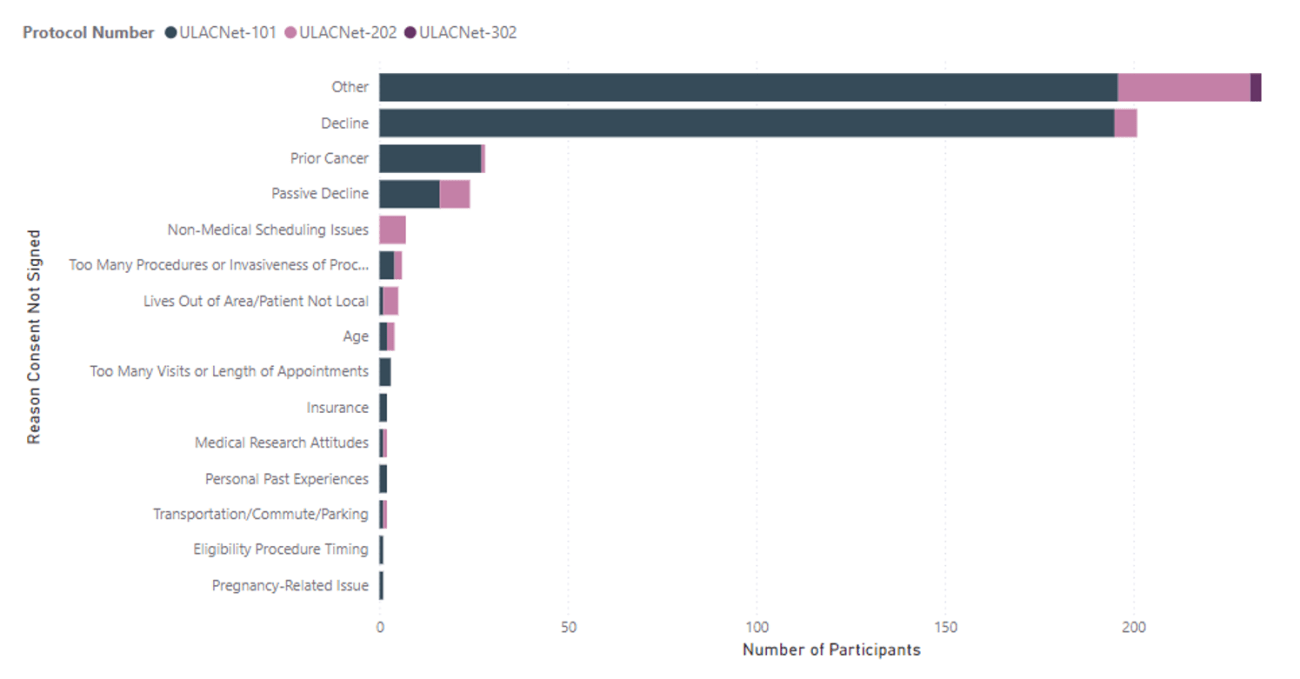
Figure 2. ULACNet Screening Studies - Reasons Individuals Did Not Sign Consent [ 3 ]
After analyzing recruitment strategies and reasons not consented, we found that AQuIP should be enhanced to better address the needs of international sites, as some recruitment strategies and reasons for participants not consenting, are not always applicable in countries outside the United States (U.S.). For example, recruitment strategies include U.S. Postal Service as an option, and reasons not consented include options such as Snowbird (those in the U.S. who move to warmer climates in the winter months). Study staff in other countries may also benefit from AQuIP data input training and improved instructions and definitions on AQuIP selections to more accurately categorize recruitment strategies and reasons for non-consent. Currently, study staff identify reasons a participant was ineligible under the ‘reasons not consented’ column; therefore, we recommend adding a new column specifically to identify reason(s) for ineligibility.
AQuIP data may also be combined with other data sources to assess per participant adverse events reported from each protocol and look at demographic data, such as gender, age, and race, of participants who have consented to participate in the study. Overall, if implemented at study sites properly, AQuIP provides a wealth of information on recruitment, enrollment, challenges, and successes at the individual-, site-, protocol-, and network-levels. We can continue to use and adapt AQuIP in order to improve clinical trial study design and maximize efficiency of participant enrollment.
About the Author

My name is Amina Chtourou, and I am a Presidential Management Fellow (PMF) at the U.S. National Cancer Institute (NCI). Prior to starting the PMF program, I received an M.P.H. in Epidemiology from the University of Pittsburgh and worked at the Allegheny County Health Department on overdose surveillance. As a PMF designated to NCI, I have had the opportunity to complete 4 rotations throughout the Institute and one developmental assignment at the U.S. Agency for International Development (USAID) over the past two years. At NCI, I rotated at the Surveillance Research Program in the Division of Cancer Control and Population Sciences, the Office of Government and Congressional Relations, the Center for Global Health, and here, at DCP. At USAID, I worked in the Global Health Bureau, Office of HIV/AIDS, Division of Strategic Information, Evaluation, and Informatics supporting the cervical cancer technical team as a data analyst/Strategic Information (SI) liaison. I also supported PEPFAR Regional Operational Planning for the Western Hemisphere Region, which consists of the Caribbean and Central and South America.
I decided to complete my final PMF rotation here at DCP to continue learning about HPV-related cancers, learn about the Program Officer (PO) role here at NIH, and what it looks like for Project Scientists and other key staff to support cooperative agreements/clinical trials networks. During my DCP rotation, I had the opportunity to learn about the grant funding cycle process and reviewed Research Performance Progress Reports (RPPRs) submitted from principal investigators (PIs) of both the ULACNet and CASCADE networks. I also completed an analysis using Accrual Quality Improvement Program, AQuIP, which DCP implemented as the accrual monitoring program for ULACNet.
Following my time at DCP, I will transition to a permanent position at NCI’s Center for Global Health. I am excited to continue to build my skills in global health and contribute to global cancer research and control. I look forward to collaborating with my DCP colleagues in the future and continue to learn about the amazing work being done in ULACNet and CASCADE.
Screening for and prevention of anal cancer as standard of care for people with HIV: the new guidelines
By: Joel Palefsky, M.D., C.M., F.R.C.P.(C)
The incidence of anal cancer is relatively low in the general population, but is substantially higher in several specific risk groups. These include individuals who are immunosuppressed due to solid organ transplant, women with a history of HPV-related cancer or pre-cancer of the cervix or vulva, and people with HIV (PWH). Men, women, and transgender individuals with HIV are all at substantially higher risk than the general population, with men who have sex with men being at the highest risk of all. In addition, all of the at-risk groups are at higher risk with older age, duration of infection, or immunosuppression. Like cervical cancer, anal cancer is associated with HPV, particularly HPV 16, and is preceded by a precancerous lesion, high-grade squamous intraepithelial lesion (HSIL). Treatment of cervical HSIL is effective in reducing the incidence of cervical cancer, and forms the basis for secondary prevention of cervical cancer with screening for cervical HSIL with cytology and/or HPV, followed by colposcopy and treatment of biopsy-proven HSIL.
Given their high incidence of anal cancer, and the similarities between cervical cancer and anal cancer, there has been interest in secondary prevention of anal cancer in the above-described risk groups. Until recently there were no formal screening programs for anal cancer or HSIL, largely due to the absence of evidence that treatment of HSIL would be effective in reducing the risk of progression to anal cancer. The ANCHOR study changed that, and showed that treatment of anal HSIL, primarily with office-based hyfrecation (a minimally invasive, safe and effective electrosurgical procedure that uses a small needle and electrical pulse to ablate lesions without cutting or suturing), reduced the incidence of anal cancer in people with HIV by 57% compared with people whose HSIL was not treated. With this new information in hand, the International Anal Neoplasia Society published screening guidelines for groups at increased risk of anal cancer, including those with HIV. On July 9, 2024, the U.S. Centers for Disease Control and Prevention, HIV Medical Association, Infectious Disease Society of America published the first federal guidelines for anal cancer prevention in people with HIV. These organizations recommend screening as standard of care in PWH (Figure 1,2), followed by high resolution anoscopy (HRA)-guided biopsy of visible lesions, and hyfrecation as first-line therapy for treatment of biopsy-proven HSIL (Figure 2).
There is still much to learn about optimal screening approaches and optimized treatment of HSIL. The currently recommended screening tests, cytology and HPV, both have limitations. Hyfrecation in the ANCHOR study did not completely prevent progression of anal HSIL to anal cancer. The ULACNet CAMPO Consortium (University of California, San Francisco, University of Puerto Rico, Instituto Nacional de Salud Publica and Instituto de Cancer Nacional) is at the forefront of addressing these issues in Latin American PWH. To enable these studies, teams at the CAMPO sites in Mexico and Puerto Rico were trained and certified in HRA. ULACNet-101 is designed to optimize screening algorithms for men and women with HIV by examining the performance of a variety of tests to detect anal HSIL and cancer. These include HPV testing, cytology, CINTec-PLUS, and methylation. The CAMPO team is also addressing therapeutic challenges; ULACNet-102 will study the safety and efficacy of a probiotic to treat anal HSIL along with associated changes is the anal microbiome. ULACNet-103 will assess different hyfrecation schedules as a means to improve hyfrecation efficacy. Together these studies will contribute to sustainable implementation of these new standard of care guidelines in Latin American PWH. They will also support a robust research capability that will contribute to the care of Latin American PWH and populations of PWH world-wide.
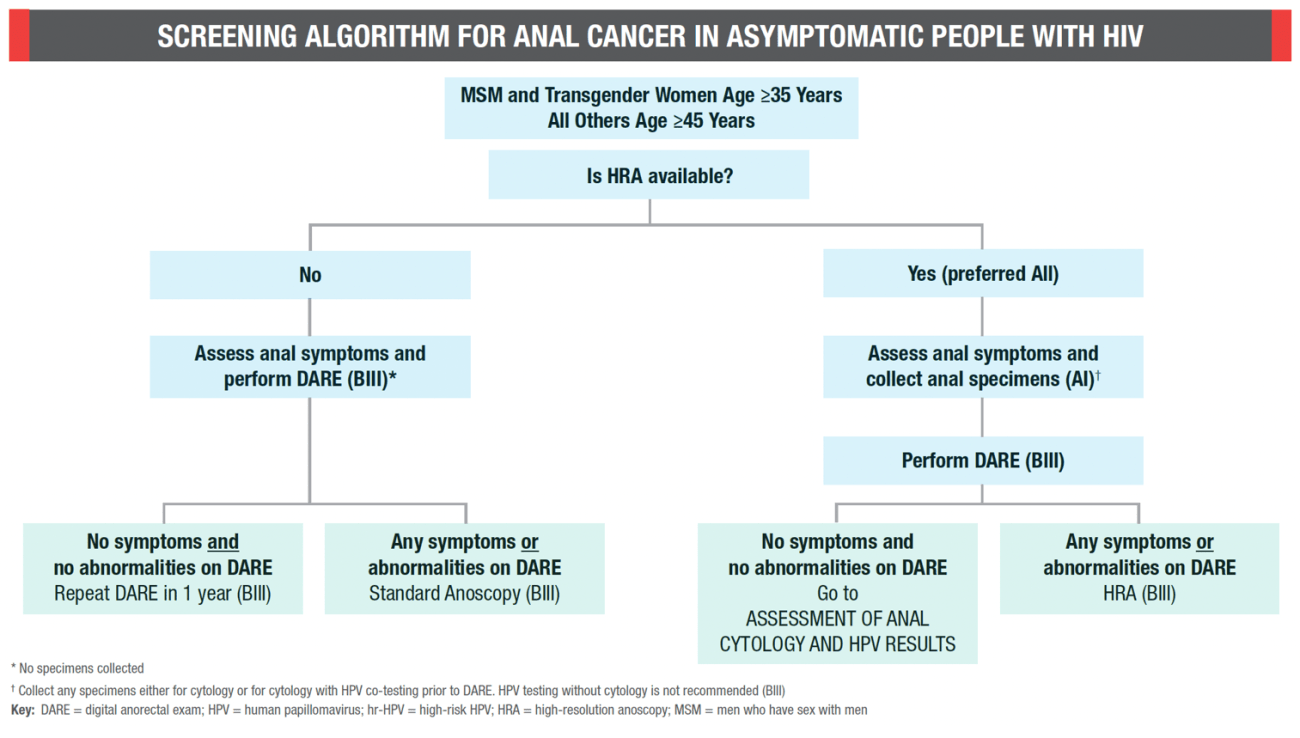
Figure 1. Screening algorithm for anal cancer in asymptomatic people with HIV [ 4 ]
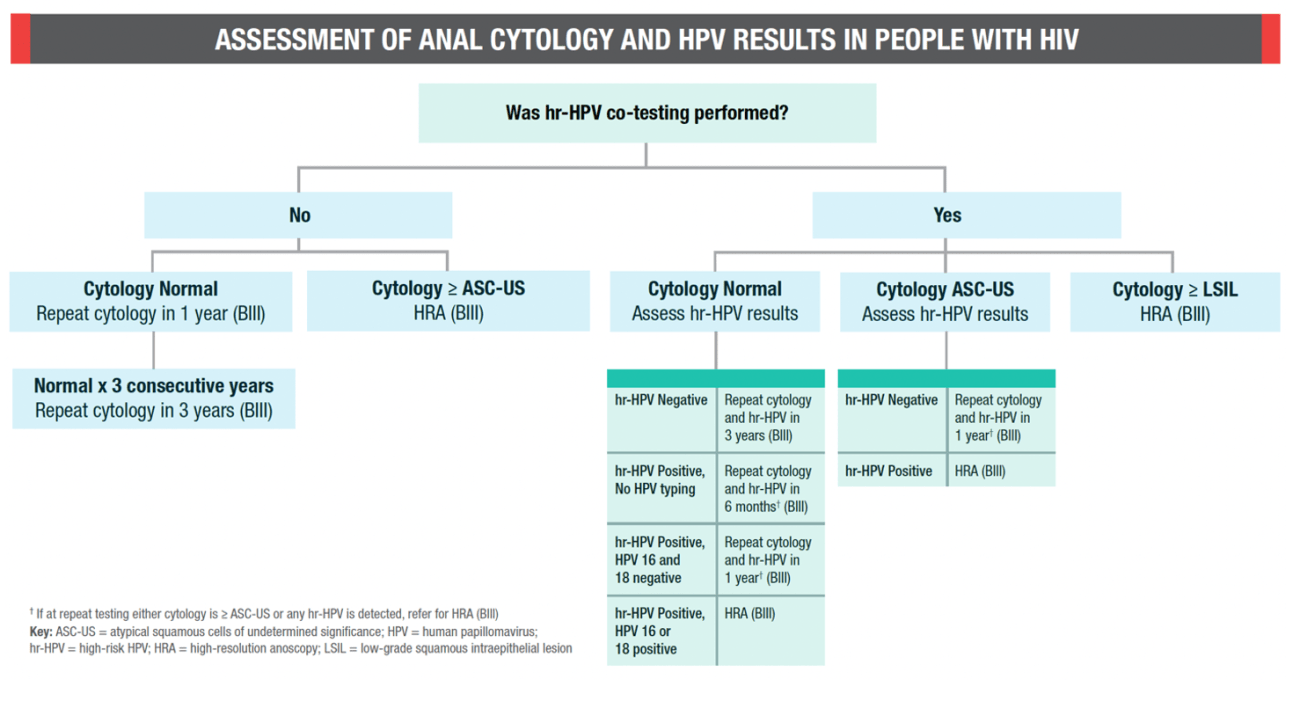
Figure 2. Assessment of anal cytology and HPV results in people with HIV [ 5 ]
Auditing The ULACNet Program: One Aspect of Quality Assurance

By: Eustaquia Chacon, B.S.
Clinical Trial Manager
Clinical Monitoring Research Program Directorate
Frederick National Laboratory for Cancer Research
and
Christian Capriolo, B.S.
Clinical Research Associate
Clinical Monitoring Research Program Directorate
Frederick National Laboratory for Cancer Research
Implementing a clinical program involves numerous processes, with quality assurance being pivotal to ensuring adherence to standards and guidelines. Within the ULACNet program, which focuses on clinical research supported by the National Cancer Institute (NCI), auditing plays a crucial role in maintaining study integrity and regulatory compliance. Auditing is conducted at two levels in the ULACNet program: at the lead academic organization (LAO) level and at the academic organization (AO) level. This article focuses on the AO level, also known as site auditing.
Importance of Auditing
Auditing is essential in the ULACNet program to upholding rigorous clinical research standards and meeting stringent NCI grant requirements. Beyond regulatory compliance, the primary objective of auditing is to protect the welfare of study participants. By systematically reviewing study procedures, audits verify protocol adherence and the implementation of quality processes outlined in ULACNet guidelines. This review process enhances the credibility and reliability of study outcomes.
The Auditing Process
Auditing within the ULACNet program is a structured and meticulous process involving several key stages:
1. Preparation
The auditing process begins with scheduling and coordinating between auditors and the AOs responsible for implementing study protocols. Auditors confirm the audit, and then review the study protocols, monitoring plan and visit reports, safety reports, and other relevant documents. Meanwhile, AOs prepare by ensuring all study data is complete, conducting internal quality checks, and addressing any previous audit findings or compliance issues. This initial phase sets the stage for effective communication and collaboration between auditors and AOs throughout the auditing process.
2. Audit Visit
Audits may be conducted on-site or remotely, depending on logistical considerations and the geographic locations of study sites within the ULACNet program (including countries like Brazil, Peru, Mexico, Haiti, Dominican Republic, and the United States). During an audit visit, auditors review all aspects of the study as per protocol requirements. This review includes verifying participant eligibility criteria, the adequacy of informed consent processes, that all study participants have signed an informed consent form, proper handling of specimens for laboratory testing, management of investigational products, documentation of regulatory approvals, and the qualifications and training of study personnel. Additionally, auditors assess how AOs communicate deviations from approved study protocols or unexpected events affecting participant safety or study objectives.
3. Audit Report and Follow-Up
After an audit, a report is written outlining the status of items audited and any identified discrepancies or areas of improvement. If issues are identified, they are communicated to the AO through an audit follow-up letter detailing the issue and suggesting corrective actions to address the findings. In the ULACNet program, the auditor generally follows up on the corrective actions taken by a site to address audit findings, but generally the site clinical research associate (CRA) is responsible for ensuring that corrective actions are implemented. Conversely, if no issues are found, the follow-up letter outlines the areas audited and affirms the audit’s completion without major concerns. These processes are critical for providing transparency and accountability, and ensuring that NCI DCP, the grant sponsor, is informed about the adherence to study protocols and regulatory standards.
Challenges in Auditing the ULACNet Program
Auditing presents challenges for both auditors and AOs involved in the ULACNet program. Auditors must navigate diverse cultural and linguistic contexts, particularly at international study sites where language barriers may complicate communication and the understanding of audit observations. Most audits in the program are done remotely, which has logistical challenges, and can hinder personal interactions and rapport-building between auditors and site personnel, potentially affecting the clarity of audit findings and the effectiveness of corrective actions.
For AOs, the audit process may represent a new and rigorous evaluation of their clinical research practices, especially if they are unfamiliar with audit procedures or have limited experience with handling regulatory inspections. This necessitates thorough preparation and coordination to ensure all study-related documentation and processes are reviewed and compliant with ULACNet and NCI guidelines.
Professional Perspective
From an auditor’s perspective, participating in the ULACNet audits represents a significant professional accomplishment. Ensuring the integrity and quality of clinical trials not only upholds ethical standards but also contributes to advancing medical research and improving health care outcomes, particularly within underserved Hispanic communities. Auditors should contribute to building a robust foundation of trust and credibility in clinical research, which is essential to fostering collaborations between researchers, institutions, and study participants.
Conclusion
Auditing within the ULACNet program is integral to maintaining the highest standards of clinical research and regulatory compliance. By systematically reviewing study protocols, procedures, and data, audits ensure that research conducted under the ULACNet program adheres to standards set forth by NCI and other regulatory bodies. As clinical research evolves, the role of auditing remains pivotal in safeguarding participant welfare, ensuring data integrity, and validating study outcomes. Through effective auditing practices, stakeholders in the ULACNet program can confidently uphold their commitment to excellence in clinical research and contribute meaningfully to advancing scientific knowledge and health care innovation.
Figure Captions
¡Bienvenido a ULACNet Update, donde compartimos actualizaciones programáticas y de investigación para la US-Latin American-Caribbean HIV/HPV-Cancer Prevention Clinical Trials Network (ULACNet)!
En esta página
- Vivir con VIH y prevenir el cáncer de cuello uterino: Lanzamiento de un estudio transformador – ULACNet 202
- Análisis del AQuIP: evaluación de la inscripción de pacientes en estudios de detección de ULACNet
- Cribado y prevención del cáncer anal como estándar de atención para personas con VIH: las nuevas pautas
- Auditoría del Programa ULACNet: Un aspecto de la garantía de calidad
Vivir con VIH y prevenir el cáncer de cuello uterino: Lanzamiento de un estudio transformador – ULACNet 202
(Consorcio ROCCHHA – Sitio México)
Por: Alejandra Portillo-Romero, M.D., Sc.D., Betania Allen-Leigh, Ph.D., Eduardo Lazcano-Ponce, M.D., Sc.D., Instituto Nacional de Salud Pública (INSP)
Reclutar mujeres que viven con el VIH para proyectos de investigación centrados en la prevención del cáncer de cuello uterino es una tarea crucial y multifacética que requiere un enfoque estratégico y sensible. Las mujeres con VIH enfrentan un riesgo significativamente mayor de desarrollar cáncer de cuello uterino debido a la mayor prevalencia de infecciones persistentes por el virus del papiloma humano (VPH). Estas infecciones, si no se detectan y tratan de manera oportuna, pueden progresar a lesiones intraepiteliales escamosas de alto grado y, eventualmente, a cáncer de cuello uterino invasivo. El estudio denominado “Optimización del cribado del cáncer de cuello uterino en mujeres que viven con VIH en países de América Latina” tiene como objetivo desarrollar una prueba de VPH de alto riesgo y una prueba molecular en el punto de atención que optimice la especificidad para detectar lesiones intraepiteliales escamosas de alto grado (CIN2+) en mujeres con VIH mientras mantiene una alta sensibilidad de la prueba.
La inscripción de mujeres con VIH en estudios de investigación presenta numerosos desafíos, incluido el estigma asociado con el VIH, información insuficiente, aceptación y participación limitadas por parte de los proveedores de atención médica, así como los obstáculos logísticos y financieros (Figura 1).
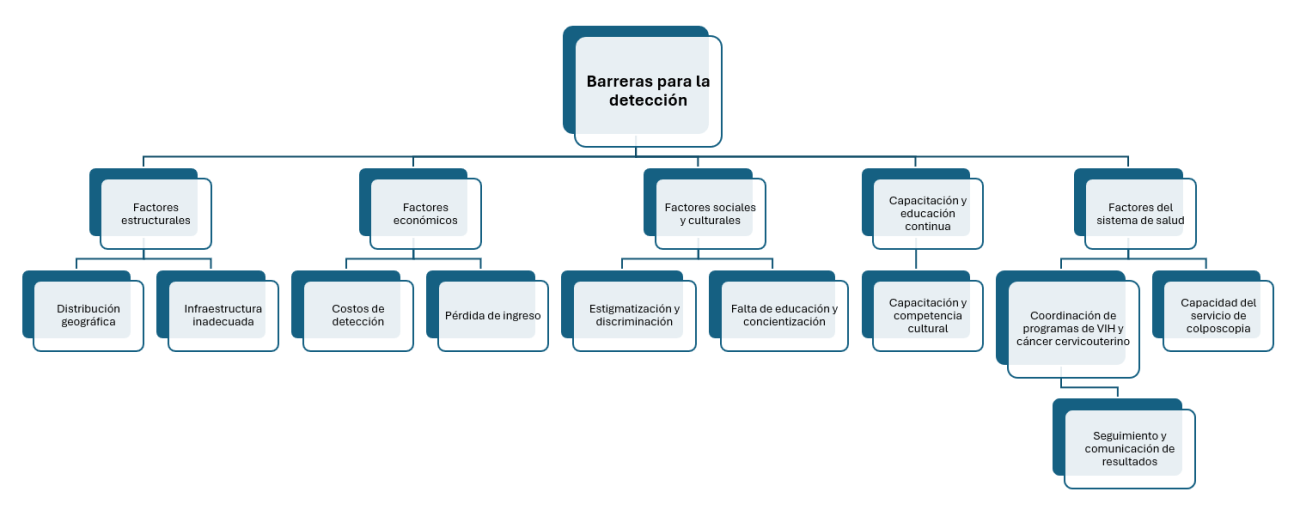
Figura 1. Barreras para la detección del VPH [ 1 ]

Conferencia "Erradicación del cáncer de cuello uterino: El caso de México", por el Dr. Eduardo Lazcano
Es esencial implementar estrategias de reclutamiento que aborden estas barreras. En el sitio México dentro de ROCCHHA, hemos abordado las barreras seleccionadas de la siguiente manera:
1. Colaboración e integración con el personal de la clínica de VIH (CAPASITS Puebla) y el Hospital de la Mujer de Puebla
Involucramos tanto al personal directivo como operativo de la clínica y al hospital para facilitar la implementación del estudio en la unidad de displasia del Hospital de la Mujer. Organizamos una presentación del proyecto en el hospital para destacar su importancia, los objetivos y beneficios para las mujeres con VIH. Durante la presentación, el Dr. Eduardo Lazcano impartió una conferencia magistral sobre "Erradicación del cáncer de cuello uterino: El caso de México”, a la que asistieron directores, médicos del hospital, residentes de ginecología, estudiantes de medicina y miembros del equipo del INSP.
2. Educación y concientización para mujeres que asisten a la clínica de VIH
Los médicos de la clínica de VIH se esfuerzan por brindar a sus pacientes que viven con VIH información clara y accesible sobre los beneficios del examen de detección del cáncer de cuello uterino en cada oportunidad durante las consultas médicas, las citas de vacunación, la administración de la terapia antirretroviral (TAR) y las visitas al laboratorio clínico. Además, un enfermero capacitado realiza sesiones informativas para los usuarios de atención médica de la clínica, para explicar la relación entre el VPH y el cáncer de cuello uterino, con el objetivo de promover la participación activa en programas de salud preventiva y promover la participación en el estudio.

Área de Displasia donde se realizan las colposcopias. Hospital de la Mujer, Puebla, México
3. Adecuación de espacios y abastecimiento de insumos médicos
La capacidad limitada de los sistemas de salud en los países de ingresos medios y bajos puede provocar retrasos en el diagnóstico y el tratamiento de lesiones precancerosas. Nuestro objetivo es optimizar el proceso de atención de la displasia para evitar que las participantes de nuestro estudio tengan que pasar por procesos administrativos complejos para obtener una colposcopia y garantizar que reciban el tratamiento en un corto plazo para minimizar así las pérdidas de seguimiento. Adicionalmente, dotamos al Hospital de la Mujer de Puebla de los insumos médicos necesarios (que muchas veces faltan) para ofrecer atención médica de mayor calidad, lo que les permite a los colposcopistas atender a un mayor número de mujeres (no limitado a las participantes del estudio).
4. Mitigar el estigma y el miedo a la discriminación entre las participantes

Katia Cruz-González (coordinadora del sitio) condujo el proceso de consentimiento informado y explicó detalladamente a las participantes las medidas de confidencialidad relativas a sus datos
Es esencial garantizar la confidencialidad de los datos de las participantes y adoptar un enfoque sensible y respetuoso hacia sus necesidades y preocupaciones. Por ello, el personal de la Clínica de VIH del Hospital de la Mujer de Puebla y del INSP se capacita continuamente para tratar con dignidad y respeto a las personas que viven con VIH. El objetivo es evitar que las mujeres se sientan juzgadas o maltratadas, y así no pierdan la oportunidad de una detección y tratamiento oportuno en caso de ser necesario. Una vez que las mujeres se inscriben en el estudio, reciben información clara y precisa sobre la protección de sus datos personales y el personal mantiene una comunicación constante hasta que reciben sus resultados.
5. Capacitación y educación continuada de los profesionales de atención a la salud
En el INSP estamos siempre comprometidos con la capacitación continua de los profesionales de la salud. A través de la colaboración con el Hospital de la Mujer de Puebla, buscamos involucrar a los residentes de ginecología, así como a los ginecólogos y colposcopistas más experimentados, en la capacitación y la investigación para fomentar mejoras en las prácticas de detección y tratamiento de lesiones precancerosas. Por ejemplo, en julio de 2024 nuestro equipo impartirá un curso en línea sobre investigación en salud pública para residentes de ginecología en el Hospital de la Mujer de Puebla.
Finalmente, participar en este ensayo no solo beneficia a las participantes al brindarles acceso a intervenciones preventivas y monitoreo médico continuo, sino que también genera conocimiento valioso que puede influir en las políticas de salud pública y mejorar los programas de prevención del cáncer cervicouterino en nuestro país, México.
Análisis del AQuIP: evaluación de la inscripción de pacientes en estudios de detección de ULACNet
Por Amina Chtourou, M.P.H.
En un esfuerzo por promover la eficiencia de la acumulación de ensayos clínicos y mejorar el reclutamiento y la retención en los estudios, se implementó el Programa de Mejoramiento de la Calidad de Acumulación (Accrual Quality Improvement Program, AQuIP) como una herramienta de monitoreo de acumulación en todos los estudios de la Red de Ensayos Clínicos de Prevención del Cáncer (ULACnet) entre Estados Unidos, América Latina y el Caribe. El programa AQuIP fue desarrollado por Ellen Richmond, M.S., GNP-BC en la División de Prevención del Cáncer (DCP) del Instituto Nacional del Cáncer y se ha utilizado en varias redes de ensayos clínicos de prevención del cáncer del DCP, incluida la ULACnet en los últimos 10 años. El AQuIP proporciona una plataforma para que el personal de investigación recopile e ingrese datos a nivel del participante a través de varias etapas del proceso de acumulación de ensayos clínicos, lo que incluye la cantidad de posibles participantes evaluados, las estrategias de reclutamiento utilizadas, la cantidad de participantes que dan su consentimiento y las razones para no dar su consentimiento o ir a la intervención. Además, el AQuIP emplea el uso de un diario del estudio para que el personal de investigación documente eventos de todo el estudio y específicos del sitio que pueden tener un impacto negativo o positivo para la acumulación. Algunos ejemplos de entradas del diario pueden incluir cambios en el número de personal del sitio (es decir, pérdida de personal o nuevas contrataciones), retrasos en la recepción del agente de estudio o suministros, problemas relacionados con el clima (como huracanes), etc. Como resultado, el AQuIP permite la identificación de posibles barreras para el reclutamiento de participantes y el potencial de modificaciones de protocolo para permitir el logro más oportuno de los objetivos relativos a los números de la inscripción.
Los datos del AQuIP se envían a la DCP mensualmente. Analizamos los datos del AQuIP para tres estudios de detección de ULACnet (ULACnet-101, ULACnet-202 y ULACnet-302), desde el inicio de la inscripción de pacientes en noviembre de 2021 hasta mayo de 2024, para comprender cómo diversos estudios han implementado el uso del AQuIP, evaluar la acumulación de participantes en los estudios de la ULACnet y evaluar la aplicabilidad del AQuIP en ensayos clínicos fuera de entornos de EE. UU.
A la fecha, en los tres estudios de detección, 1988 individuos han firmado el consentimiento y 1965 han iniciado la intervención del estudio, como se muestra en la Tabla 1.
| Número de estudio | Número de consentimientos firmados | Número de intervenciones iniciadas en el estudio | Inscripción objetivo | Estado del estudio |
|---|---|---|---|---|
| ULACNet-101 | 1,107 | 1,106 | 1,500 | En curso |
| ULACNet-202 | 252 | 251 | 1,000 | En curso |
| ULACNet-302 | 629 | 608 | 600 | Inscripción completada |
| Total | 1,988 | 1,965 | 3,100 |
Las estrategias de reclutamiento más comunes en los tres estudios de selección fueron “otras” estrategias, derivaciones de médicos y derivaciones a través del personal dentro de la institución que no era personal del estudio. La figura 1 a continuación muestra las estrategias de reclutamiento empleadas en los tres estudios de detección. Por “razones de no consentimiento”, el personal del estudio a menudo reportó “otra” razón, un individuo declinó o un individuo tenía un cáncer previo. La figura 2 a continuación muestra “razones de no consentimiento” en los tres estudios de detección. La figura 2 está restringida a las personas que fueron contactadas pero que no dieron su consentimiento para unirse al estudio y no refleja necesariamente las razones por las que los participantes no fueron elegibles para iniciar la intervención del estudio después de firmar el formulario de consentimiento.

Figura 1. Estrategias de reclutamiento de participantes para estudios de detección de la ULACNet [ 2 ]

Figura 2. Estudios de detección de ULACNet: razones por las que las personas no firman el consentimiento [ 3 ]
Después de analizar las estrategias de reclutamiento y las razones no consentidas, encontramos que el AQuIP debería mejorarse para atender mejor las necesidades de los sitios internacionales, ya que algunas estrategias de reclutamiento y razones por las cuales los participantes no consintieron no siempre son aplicables en países fuera de Estados Unidos (EE. UU.). Por ejemplo, las estrategias de reclutamiento incluyen el servicio postal de EE. UU. como opción, y las razones de no consentimiento incluyen opciones como Snowbird (aquellas personas de Estados Unidos que se mudan a climas más cálidos en los meses de invierno). El personal del estudio de otros países también puede beneficiarse de la capacitación de entrada de datos del AQuIP y de las instrucciones y definiciones mejoradas sobre las selecciones del AQuIP para categorizar con mayor precisión las estrategias de reclutamiento y las razones del no consentimiento. Actualmente, el personal del estudio identifica las razones por las que un participante no fue elegible en la columna “razones de no consentimiento”, por lo tanto, recomendamos agregar una nueva columna específicamente para identificar las razones de inelegibilidad.
Los datos del AQuIP también pueden combinarse con otras fuentes de datos para evaluar los eventos adversos reportados por participante de cada protocolo y observar datos demográficos, como sexo, edad y raza, de los participantes que han dado su consentimiento para participar en el estudio. En general, si se implementa correctamente en los sitios de estudio, el AQuIP proporciona una gran cantidad de información sobre reclutamiento, inscripción, desafíos y éxitos a nivel individual, sitio, protocolo y red. Podemos seguir utilizando y adaptando el AQuIP con el fin de mejorar el diseño del estudio de ensayos clínicos y maximizar la eficiencia de la inscripción de participantes.
Sobre el autor

Mi nombre es Amina Chtourou y soy Miembro de la Administración Presidencial (PMF) en el Instituto Nacional del Cáncer (NCI) de EE. UU. Antes de iniciar el programa de PMF, recibí un M.P.H. en Epidemiología de la Universidad de Pittsburgh y trabajé en el Departamento de Salud del Condado de Allegheny, en vigilancia de sobredosis. Como PMF designada del NCI, he tenido la oportunidad de completar 4 rotaciones en todo el instituto y una asignación de desarrollo en la Agencia para el Desarrollo Internacional de EE. UU. (USAID) en los últimos dos años. En el NCI, roté en el Programa de Investigación de Vigilancia en la División de Control del Cáncer y Ciencias de la Población, la Oficina de Relaciones Gubernamentales y Congresales, el Centro de Salud Global, y aquí, en la DCP. En USAID, trabajé en la Oficina de Salud Global, Oficina de VIH/SIDA, División de Información Estratégica, Evaluación e Informática para apoyar al equipo técnico del cáncer de cuello uterino como intermediaria/analista de Información Estratégica (SI). También apoyé la Planificación Operativa Regional PEPFAR para la Región del Hemisferio Occidental, que consiste en el Caribe y América Central y del Sur.
Decidí completar mi rotación final de PMF aquí en la DCP para continuar aprendiendo sobre los cánceres relacionados con el VIH, aprender sobre el rol de Oficial de Programas (PO) aquí en los NIH y acerca de la manera en que los Científicos de Proyectos y otro personal clave perciben el apoyo de acuerdos cooperativos/redes de ensayos clínicos. Durante mi rotación en la DCP, tuve la oportunidad de conocer el proceso del ciclo de financiamiento de subvenciones y revisé los Informes de Progreso de Desempeño de Investigación (RPPR) enviados por investigadores principales (PI) de las redes ULACnet y CASCADE. También completé un análisis usando el Programa de Mejoramiento de la Calidad de Acumulación, AQuIP, el cual la DCP implementó como el programa de monitoreo de acumulación para ULACnet.
Después de mi etapa en la DCP, pasaré a un puesto permanente en el Centro para la Salud Global del NCI. Estoy emocionada por seguir desarrollando mis habilidades en la salud global y contribuir con la investigación y el control del cáncer en el mundo. Espero poder colaborar con mis colegas de la DCP en el futuro y seguir aprendiendo sobre el increíble trabajo que se está realizando en ULACnet y CASCADE.
Cribado y prevención del cáncer anal como estándar de atención para personas con VIH: las nuevas pautas
Par: Joel Palefsky, M.D., C.M., F.R.C.P.(C)
La incidencia de cáncer anal es relativamente baja en la población general, pero es sustancialmente mayor en varios grupos de riesgo específicos. Estos incluyen individuos inmunodeprimidos debido a un trasplante de órganos sólidos, mujeres con antecedentes de cáncer relacionado con el VHP o precáncer de cuello uterino o vulva, y personas con VIH (PWH). Los hombres, las mujeres y las personas transgénero con VIH corren un riesgo sustancialmente mayor que la población general, y los hombres que tienen relaciones sexuales con hombres corren el mayor riesgo de todos. Además, todos los grupos en riesgo están en mayor riesgo con la edad avanzada, la duración de la infección o la inmunosupresión. Al igual que el cáncer cervical, el cáncer anal se asocia con el VPH, particularmente el VPH 16, y está precedido por una lesión precancerosa, lesión intraepitelial escamosa de alto grado (HSIL). El tratamiento del HSIL cervical es eficaz para reducir la incidencia del cáncer cervical, y forma la base para la prevención secundaria del cáncer cervical con cribado de HSIL cervical con citología y/o VPH, seguido de la colposcopia y el tratamiento del HSIL probado por biopsia.
Dada su alta incidencia de cáncer anal, y las similitudes entre el cáncer cervical y el cáncer anal, ha habido interés en la prevención secundaria del cáncer anal en los grupos de riesgo descritos anteriormente. Hasta hace poco no existían programas formales de cribado para el cáncer anal o HSIL, en gran parte debido a la ausencia de evidencia de que el tratamiento del HSIL sería efectivo para reducir el riesgo de progresión al cáncer anal. El estudio ANCHOR cambió eso, y mostró que el tratamiento del HSIL anal, principalmente con hifrecación basada en el consultorio (un procedimiento electroquirúrgico mínimamente invasivo, seguro y eficaz que utiliza una aguja pequeña y pulso eléctrico para realizar una ablación de lesiones sin cortar ni suturar), redujo la incidencia de cáncer anal en personas con VIH en un 57 % en comparación con personas cuyo HSIL no fue tratado. Con esta nueva información, la Sociedad Internacional de Neoplasia Anal publicó las pautas de cribado para grupos con mayor riesgo de cáncer anal, incluyendo aquellos con VIH. El 9 de julio de 2024, los Centros para el Control y la Prevención de Enfermedades de EE. UU., la HIV Medical Association y la Infectious Disease Society of America publicaron las primeras pautas federales para la prevención del cáncer anal en personas con VIH. Estas organizaciones recomiendan el cribado como estándar de atención para PWH (Figura 1,2), seguido de biopsia guiada por una anoscopia de alta resolución (HRA) de lesiones visibles, y la hifrecación como terapia de primera línea para el tratamiento del HSIL probado por biopsia (Figura 2).
Todavía queda mucho por aprender sobre los enfoques óptimos de cribado y el tratamiento optimizado del HSIL. Las pruebas de cribado actualmente recomendadas, citología y VPH, tienen limitaciones. La hifrecación en el estudio ANCHOR no evitó completamente la progresión de HSIL anal a cáncer anal. El Consorcio ULACnet CAMPO (Universidad de California, San Francisco, Universidad de Puerto Rico, Instituto Nacional de Salud Pública e Instituto de Cáncer Nacional) está a la vanguardia del tratamiento de estas cuestiones para las PWH latinoamericanas. Para posibilitar estos estudios, los equipos de los sitios de CAMPO en México y Puerto Rico fueron capacitados y certificados en HRA. ULACnet-101 está diseñado para optimizar los algoritmos de detección para hombres y mujeres con VIH mediante el examen de la realización de una variedad de pruebas para detectar HSIL anal y cáncer. Estos incluyen pruebas de VPH, citología, CINTEC-plus y metilación. El equipo de CAMPO también está abordando retos terapéuticos; ULACnet-102 estudiará la seguridad y eficacia de un probiótico para tratar el HSIL anal junto con los cambios asociados es el microbioma anal. ULACnet-103 evaluará diferentes programas de hifrecación como un medio para mejorar la eficacia de la hifrecación. En conjunto, estos estudios contribuirán a la implementación sostenible de estas nuevas pautas de estándar de atención para las PWH latinoamericanas. También apoyarán una sólida capacidad de investigación que contribuirá a la atención de las PWH latinoamericanas y de las poblaciones de PWH en todo el mundo.

Figura 1. Algorithme de dépistage du cancer de l'anus chez les personnes séropositives asymptomatiques [ 4 ]

Figura 2. Évaluation des résultats de la cytologie anale et du VPH chez les personnes séropositives [ 5 ]
Auditoría del Programa ULACNet: Un aspecto de la garantía de calidad

Por: Eustaquia Chacon, B.S.
Gerente de Ensayos Clínicos
Dirección del Programa de Investigación de Monitoreo Clínico
Laboratorio Nacional Frederick para la Investigación del Cáncer
y
Christian Capriolo, B.S.
Asociado de Investigación Clínica
Dirección del Programa de Investigación de Monitoreo Clínico
Laboratorio Nacional Frederick para la Investigación del Cáncer
La implementación de un programa clínico implica numerosos procesos, siendo la garantía de la calidad fundamental para asegurar el cumplimiento de los estándares y las pautas. Dentro del programa ULACNet, que se centra en la investigación clínica respaldada por el Instituto Nacional del Cáncer (NCI), la auditoría juega un papel crucial en el mantenimiento de la integridad del estudio y el cumplimiento normativo. La auditoría se realiza en dos niveles en el programa ULACNet: a nivel de organización académica líder (LAO) y a nivel de organización académica (AO). Este artículo se centra en el nivel AO, también conocido como auditoría del sitio.
Importancia de la auditoría
La auditoría es esencial en el programa ULACNet para sostener rigurosos estándares de investigación clínica y cumplir con los estrictos requisitos de subvención del NCI. Más allá del cumplimiento normativo, el objetivo principal de la auditoría es proteger el bienestar de los participantes en el estudio. Al revisar sistemáticamente los procedimientos de estudio, las auditorías verifican la adherencia al protocolo y la implementación de los procesos de calidad delineados en los lineamientos de ULACNet. Este proceso de revisión mejora la credibilidad y confiabilidad de los resultados del estudio.
El proceso de auditoría
La auditoría dentro del programa ULACNet es un proceso estructurado y meticuloso que involucra varias etapas clave:
1. Preparación
'El proceso de auditoría comienza con la programación y coordinación entre los auditores y las AO responsables de implementar los protocolos de estudio. Los auditores confirman la auditoría, para luego revisar los protocolos de estudio, plan de monitoreo y reportes de visitas, informes de seguridad, y otros documentos relevantes. Mientras tanto, las AO se preparan asegurando que todos los datos del estudio estén completos, realizando controles de calidad internos y abordando cualquier hallazgo de auditoría anterior o problemas de cumplimiento. Esta fase inicial prepara el escenario para una comunicación y colaboración efectivas entre auditores y las AO a lo largo del proceso de auditoría.
2. Visita de auditoría
Las auditorías pueden realizarse en el sitio o de forma remota, dependiendo de consideraciones logísticas y de la ubicación geográfica de los sitios de estudio dentro del programa ULACNet (incluidos países como Brasil, Perú, México, Haití, República Dominicana y Estados Unidos). Durante una visita de auditoría, los auditores revisan todos los aspectos del estudio según los requisitos del protocolo. Esta revisión incluye verificar los criterios de elegibilidad de los participantes, la adecuación de los procesos de consentimiento informado, que todos los participantes del estudio hayan firmado un formulario de consentimiento informado, el manejo adecuado de las muestras para pruebas de laboratorio, manejo de productos en investigación, documentación de aprobaciones regulatorias y las calificaciones y capacitación del personal del estudio. Además, los auditores evalúan cómo las AO comunican desviaciones de protocolos de estudio aprobados o eventos inesperados que afectan la seguridad de los participantes o los objetivos del estudio.
3. Informe de auditoría y seguimiento
Después de una auditoría, se escribe un informe que describe el estado de los elementos auditados y cualquier discrepancia o áreas de mejora identificadas. Si se identifican problemas, se comunican a la AO a través de una carta de seguimiento de auditoría detallando el problema y sugiriendo acciones correctivas para abordar los hallazgos. En el programa ULACNet, el auditor generalmente da seguimiento a las acciones correctivas que toma un sitio para abordar los hallazgos de la auditoría, pero generalmente el asociado de investigación clínica (CRA) del sitio es responsable de asegurar que se implementen las acciones correctivas. Por el contrario, si no se encuentran problemas, la carta de seguimiento describe las áreas auditadas y afirma la finalización de la auditoría sin mayores problemas. Estos procesos son críticos para proporcionar transparencia y rendición de cuentas, y garantizar que el NCI DCP, el patrocinador de la subvención, esté informado sobre el cumplimiento de los protocolos de estudio y las normas regulatorias.
Desafíos en la Auditoría del Programa ULACNet
La auditoría presenta desafíos tanto para los auditores como para las AO involucrados en el programa ULACNet. Los auditores deben navegar por diversos contextos culturales y lingüísticos, particularmente en sitios de estudio internacionales donde las barreras lingüísticas pueden complicar la comunicación y la comprensión de las observaciones de auditoría. La mayoría de las auditorías en el programa se realizan de forma remota, lo que tiene desafíos logísticos, y puede dificultar las interacciones personales y la creación de relaciones entre los auditores y el personal del sitio, lo que podría afectar la claridad de los hallazgos de la auditoría y la efectividad de las acciones correctivas.
Para las AO, el proceso de auditoría puede representar una evaluación nueva y rigurosa de sus prácticas de investigación clínica, especialmente si no están familiarizados con los procedimientos de auditoría o tienen experiencia limitada en el manejo de inspecciones reglamentarias. Esto requiere una preparación y coordinación minuciosas para garantizar que toda la documentación y los procesos relacionados con el estudio sean revisados y cumplan con los lineamientos de ULACNet y NCI.
Perspectiva profesional
Desde la perspectiva de un auditor, participar en las auditorías ULACNet representa un logro profesional significativo. Garantizar la integridad y calidad de los ensayos clínicos no solo defiende los estándares éticos, sino que también contribuye a avanzar en la investigación médica y mejorar los resultados de la atención médica, particularmente dentro de las comunidades hispanas desatendidas. Los auditores deben contribuir a construir una base sólida de confianza y credibilidad en la investigación clínica, lo cual es esencial para fomentar la colaboración entre investigadores, instituciones y participantes en el estudio.
Conclusión
La auditoría dentro del programa ULACNet es integral para mantener los más altos estándares de investigación clínica y cumplimiento normativo. Al revisar sistemáticamente los protocolos, procedimientos y datos del estudio, las auditorías aseguran que la investigación realizada bajo el programa ULACNet se adhiera a los estándares establecidos por el NCI y otros organismos reguladores. A medida que evoluciona la investigación clínica, el papel de la auditoría sigue siendo fundamental para salvaguardar el bienestar de los participantes, garantizar la integridad de los datos y validar los resultados del estudio. A través de prácticas efectivas de auditoría, las partes interesadas en el programa ULACNet pueden mantener con confianza su compromiso con la excelencia en la investigación clínica y contribuir de manera significativa al avance del conocimiento científico y a la innovación en el cuidado de la salud.
Leyendas de figuras
Bienvenue dans la mise à jour ULACNet Update, où nous partageons des mises à jour programmatiques et de recherche pour le réseau d'essais cliniques sur la US-Latin American-Caribbean HIV/HPV-Cancer Prevention Clinical Trials Network (ULACNet)!
Nesta página
- Vivendo com o HIV e prevenindo o câncer do colo do útero: Lançamento de um estudo transformador - ULACNet 202
- Análise AQuIP: Avaliando o recrutamento de pacientes em estudos de rastreamento da ULACNet
- Cribado y prevención del cáncer anal como estándar de atención para personas con VIH: las nuevas pautas
- Auditoria do Programa ULACNet: Um aspecto da garantia de qualidade
Vivendo com o HIV e prevenindo o câncer do colo do útero: Lançamento de um estudo transformador - ULACNet 202
(Associação ROCCHHA - Centro de estudos do México)
Por: Alejandra Portillo-Romero, Médica, Doutora em Ciências, Betania Allen-Leigh, Doutora em Filosofia, Eduardo Lazcano-Ponce, Médico, Doutor em Ciências, Instituto Nacional de Saúde Pública (INSP, na sigla em inglês)
O recrutamento de mulheres vivendo com HIV (WLHIV, na sigla em inglês) para projetos de pesquisa voltados à prevenção do câncer do colo do útero é uma tarefa crucial e multifacetada que exige uma abordagem estratégica e sensível. WLHIV enfrentam um risco significativamente maior de desenvolver câncer do colo do útero devido à maior prevalência de infecções persistentes pelo papilomavírus humano (HPV). Essas infecções, se não forem detectadas e tratadas a tempo, podem evoluir para lesões intraepiteliais escamosas de alto grau (HSIL, na sigla em inglês) e, eventualmente, para um câncer invasivo do colo do útero. O estudo denominado “Optimization of Cervical Cancer Screening among Women Living with HIV in Latin American Countries” (Otimização do Rastreamento do Câncer do Colo do Útero entre Mulheres Vivendo com HIV em Países da América Latina) tem como objetivo desenvolver um teste de HPV de alto risco e um teste molecular no ponto de atendimento (point-of-care) que otimize a especificidade para detectar HSIL (CIN2+) em WLHIV, mantendo alta sensibilidade do teste.
O recrutamento de WLHIV em estudos de pesquisa apresenta vários desafios, incluindo o estigma associado ao HIV, informações insuficientes, aceitação e participação limitadas dos profissionais de saúde, além de obstáculos logísticos e financeiros (Figura 1).
Figura 1. Obstáculos para a realização do rastreamento do HPV [ 1 ]

Palestra "Erradicação do Câncer do Colo do Útero: O case do México", por Dr. Eduardo Lazcano
É essencial implementar estratégias de recrutamento que abordem estes obstáculos. No centro de estudo do México dentro da ROCCHHA, abordamos os obstáculos selecionados da seguinte forma:
1. Colaboração e integração com a clínica de HIV (CAPASITS Puebla) e a equipe do Hospital da Mulher de Puebla
Envolvemos tanto a equipe gerencial quanto a operacional da clínica e do hospital para facilitar a implementação do estudo na unidade de displasia do Hospital da Mulher. Organizamos uma apresentação do projeto no hospital, destacando a importância, os objetivos e os benefícios para as WLHIV. Durante a apresentação, o Dr. Eduardo Lazcano fez a palestra principal sobre "Erradicação do Câncer do Colo do Útero: O case do México", com a presença de diretores, médicos do hospital, residentes de ginecologia, estudantes de medicina e membros da equipe do INSP.
2. Educação e conscientização para mulheres que frequentam a clínica de HIV
Os médicos da clínica de HIV se esforçam para fornecer às pacientes vivendo com HIV informações claras e acessíveis sobre os benefícios do exame de colo do útero, aproveitando todas as oportunidades durante as consultas médicas, consultas de vacinação, administração de terapia antirretroviral (ART, na sigla em inglês) e visitas aos laboratórios clínicos. Além disso, uma enfermeira treinada realiza sessões informativas para os pacientes da clínica, explicando a relação entre HPV e câncer do colo do útero, com o objetivo de promover a participação ativa em programas de saúde preventiva e incentivar o envolvimento no estudo.

Área de Displasias onde as colposcopias são realizadas. Hospital da Mulher, Puebla, México
3. Adequação dos espaços e fornecimento de suprimentos médicos
A capacidade limitada dos sistemas de saúde em países de renda média e baixa pode levar a atrasos no diagnóstico e no tratamento de lesões pré-cancerosas. Nosso objetivo é otimizar o processo de tratamento da displasia para evitar que as participantes do nosso estudo passem por processos administrativos complexos para obter uma colposcopia e garantir que recebam o tratamento em um curto intervalo de tempo, minimizando assim a perda de acompanhamento. Além disso, fornecemos ao Hospital da Mulher de Puebla os suprimentos médicos necessários (que frequentemente estão em falta) para oferecer um atendimento médico de maior qualidade, permitindo que os colposcopistas atendam a um número maior de mulheres (não se limitando apenas às participantes do estudo).
4. Mitigar o estigma e o medo da discriminação entre as participantes

Katia Cruz-González (Coordenadora do local) conduziu o processo de consentimento informado, explicando detalhadamente às participantes as medidas de confidencialidade relacionadas aos dados pessoais
É essencial garantir a confidencialidade dos dados das participantes e adotar uma abordagem sensível e respeitosa em relação às necessidades e preocupações delas. Portanto, a equipe da clínica de HIV, do Hospital da Mulher de Puebla e do INSP recebe treinamento contínuo sobre como tratar as pessoas vivendo com HIV com dignidade e respeito. O objetivo é evitar que as mulheres se sintam julgadas ou maltratadas, garantindo assim que elas não percam a chance de detecção e tratamento precoces, se necessário. Depois que as mulheres são inscritas no estudo, elas recebem informações claras e precisas sobre a proteção dos respectivos dados pessoais, e a equipe mantém uma comunicação constante até que elas recebam os resultados.
5. Treinamento e instrução contínuos para profissionais de saúde
No INSP, estamos sempre comprometidos com a educação contínua dos profissionais de saúde. Por meio da colaboração com o Hospital da Mulher de Puebla, nosso objetivo é envolver residentes de ginecologia, bem como ginecologistas e colposcopistas mais experientes, em treinamento e pesquisa, incentivando melhorias nas práticas de triagem e no tratamento de lesões pré-cancerosas. Por exemplo, em julho de 2024, os membros da nossa equipe ministrarão um curso online sobre pesquisa em saúde pública para residentes de ginecologia no Hospital da Mulher de Puebla.
Por fim, a participação nesse estudo não só beneficia as participantes ao fornecer acesso a intervenções preventivas e monitoramento médico contínuo, mas também gera conhecimento valioso que pode influenciar as políticas de saúde pública e aprimorar os programas de prevenção do câncer do colo do útero em nosso país, México.
Análise AQuIP: Avaliando o recrutamento de pacientes em estudos de rastreamento da ULACNet
Por: Amina Chtourou, Mestre em Saúde Pública
Com o objetivo de promover a eficiência na captação de pacientes para ensaios clínicos e melhorar o recrutamento e a retenção de participantes nos estudos, o Programa de Melhoria da Qualidade de Captação (AQuIP, na sigla em inglês) foi implementado como uma ferramenta de monitoramento de captação em todos os estudos da Rede de Ensaios Clínicos de Prevenção de Cânceres Associados ao HIV/HPV dos EUA-América Latina-Caribe (ULACNet, na sigla em inglês). O programa AQuIP foi desenvolvido por Ellen Richmond, Mestre em Ciências, Enfermeira Especialista em Geriatria Certificada, na Divisão de Prevenção do Câncer (DCP, na sigla em inglês) do Instituto Nacional do Câncer e tem sido utilizado em várias redes de ensaios clínicos de prevenção do câncer da DCP, incluindo a ULACNet, nos últimos 10 anos. O AQuIP fornece uma plataforma para que a equipe de pesquisa colete e insira dados dos participantes em vários estágios do processo de captação dos ensaios clínicos, incluindo o número de potenciais participantes examinados, as estratégias de recrutamento utilizadas, o número de participantes que assinaram o consentimento, e os motivos para não consentirem ou não prosseguirem com a intervenção. Além disso, o AQuIP utiliza um diário de estudo para que a equipe de pesquisa documente eventos específicos do local e de todo o estudo que podem impactar positiva ou negativamente a captação de participantes. Exemplos de registros no diário podem incluir alterações no número de funcionários do centro (ou seja, perda de funcionários ou novas contratações), atrasos no recebimento de agentes ou suprimentos do estudo, problemas relacionados ao clima (por exemplo, furacão), etc. Como resultado, o AQuIP permite a identificação de possíveis obstáculos ao recrutamento de participantes e a possibilidade de modificações no protocolo para possibilitar a conclusão mais oportuna dos números de inscrição desejados.
Os dados do AQuIP são enviados mensalmente à DCP. Analisamos os dados do AQuIP de três estudos de rastreamento da ULACNet (ULACNet-101, ULACNet-202 e ULACNet-302), desde o início do recrutamento de pacientes em novembro de 2021 até maio de 2024, para entender como diferentes estudos implementaram o uso do AQuIP, avaliar a captação de participantes nos estudos da ULACNet e verificar a aplicabilidade do AQuIP em ensaios clínicos fora dos Estados Unidos.
Até o momento, nos três estudos de rastreamento, 1.988 indivíduos assinaram o consentimento e 1.965 iniciaram a intervenção do estudo, conforme mostrado na Tabela 1.
| Número do estudo | Número de consentimentos assinados | Número de pessoas que iniciaram a intervenção do estudo | Meta de recrutamento | Status do estudo |
|---|---|---|---|---|
| ULACNet-101 | 1,107 | 1,106 | 1,500 | em andamento |
| ULACNet-202 | 252 | 251 | 1,000 | em andamento |
| ULACNet-302 | 629 | 608 | 600 | Recrutamento concluído |
| Total | 1,988 | 1,965 | 3,100 |
As estratégias de recrutamento mais comuns em todos os três estudos de rastreamento foram "outras" estratégias, encaminhamentos médicos e encaminhamentos por meio de funcionários da instituição que não faziam parte da equipe do estudo. A Figura 1 abaixo mostra as estratégias de recrutamento empregadas nos três estudos de rastreamento. Em relação aos ‘motivos para não consentir’, a equipe do estudo frequentemente relatou um ‘outro’ motivo, o indivíduo recusou ou o indivíduo teve um câncer anterior. A Figura 2 abaixo mostra os ‘motivos para não consentir’ nos três estudos de rastreamento. A Figura 2 se restringe aos indivíduos que foram contatados, mas não consentiram em participar do estudo e não reflete necessariamente os motivos pelos quais os participantes não eram elegíveis para iniciar a intervenção do estudo depois de assinarem o formulário de consentimento.

Figura 1. Estratégias de recrutamento de participantes nos estudos de rastreamento da ULACNet [ 2 ]

Figura 2. Estudos de rastreamento da ULACNet - Motivos pelos quais os indivíduos não assinaram o consentimento [ 3 ]
Após analisar as estratégias de recrutamento e os motivos para não consentir, descobrimos que o AQuIP deve ser aprimorado para melhor atender às necessidades dos centros internacionais, pois algumas estratégias de recrutamento e motivos para os participantes não consentirem nem sempre são aplicáveis em países fora dos Estados Unidos (EUA). Por exemplo, as estratégias de recrutamento incluem o Serviço Postal dos EUA como uma opção, e os motivos para não consentimento incluem opções como Snowbird (pessoas que vivem nos EUA e que se mudam para climas mais quentes nos meses de inverno). A equipe de estudo em outros países também pode se beneficiar de um treinamento sobre a inserção de dados no AQuIP e de instruções e definições aprimoradas sobre as seleções do AQuIP para categorizar mais precisamente as estratégias de recrutamento e os motivos para não consentimento. Atualmente, a equipe do estudo identifica os motivos pelos quais um participante não seria elegível na coluna ‘motivos para não consentir’; portanto, recomendamos a adição de uma nova coluna especificamente para identificar os motivos para a inelegibilidade.
Os dados do AQuIP também podem ser combinados com outras fontes de dados para avaliar eventos adversos relatados por participante de cada protocolo e analisar dados demográficos, como gênero, idade e raça, dos participantes que consentiram em participar do estudo. De modo geral, se implementado adequadamente nos centros de estudo, o AQuIP fornece uma grande quantidade de informações sobre recrutamento, inscrição, desafios e sucessos nos níveis individual, do centro, do protocolo e da rede. Podemos continuar a usar e adaptar o AQuIP para melhorar o planejamento dos estudos clínicos e maximizar a eficiência do recrutamento de participantes.
Sobre a autora

Meu nome é Amina Chtourou e sou uma Fellow de Gestão Presidencial (PMF, na sigla em inglês) no Instituto Nacional do Câncer (NCI, na sigla em inglês) dos EUA. Antes de iniciar o programa PMF, eu recebi um Mestrado em Saúde Pública em Epidemiologia pela Universidade de Pittsburgh e trabalhei no Departamento de Saúde do Condado de Allegheny com vigilância de overdoses. Como Fellow de Gestão Presidencial designada ao NCI, tive a oportunidade de realizar 4 rotações ao longo do Instituto e uma atribuição de desenvolvimento na Agência dos EUA para o Desenvolvimento Internacional (USAID, na sigla em inglês) nos últimos dois anos. No NCI, realizei rotações no Programa de Pesquisa em Vigilância na Divisão de Controle do Câncer e Ciências Populacionais, no Escritório de Relações Governamentais e Congressuais, no Centro para Saúde Global, e aqui, na DCP. Na USAID, trabalhei no Escritório de Saúde Global, Escritório de HIV/AIDS, Divisão de Informação Estratégica, Avaliação e Informática, apoiando a equipe técnica de câncer do colo do útero como analista de dados e interlocutora de Informação Estratégica (SI, na sigla em inglês). Também apoiei o Planejamento Operacional Regional do Plano de Emergência do Presidente para o Alívio da AIDS (PEPFAR, na sigla em inglês) para a região do Hemisfério Ocidental, que consiste no Caribe e nas Américas Central e do Sul.
Decidi realizar minha última rotação do PMF aqui na DCP para continuar aprendendo sobre cânceres relacionados ao HPV, entender o papel de Oficial de Programa (PO, na sigla em inglês) no Instituto Nacional de Saúde (NIH, na sigla em inglês) e observar como os Cientistas de Projeto e outros membros essenciais da equipe apoiam acordos cooperativos e redes de ensaios clínicos. Durante minha rotação na DCP, tive a oportunidade de aprender sobre o processo do ciclo de financiamento de subsídios e analisei os Relatórios de Progresso do Desempenho em Pesquisa (RPPRs, na sigla em inglês) enviados pelos pesquisadores principais (PIs, na sigla em inglês) das redes ULACNet e CASCADE. Também concluí uma análise utilizando o Programa de Melhoria da Qualidade de Captação (AQuIP), que a DCP implementou como o programa de monitoramento de captação para a ULACNet.
Após meu período na DCP, farei a transição para uma posição permanente no Centro para Saúde Global do NCI. Estou animada para continuar desenvolvendo minhas habilidades em saúde global e contribuir para a pesquisa e controle do câncer em nível global. Estou ansiosa para colaborar com meus colegas da DCP no futuro e continuar aprendendo sobre o trabalho incrível sendo realizado na ULACNet e na CASCADE.
Cribado y prevención del cáncer anal como estándar de atención para personas con VIH: las nuevas pautas
Por: Joel Palefsky, M.D., C.M., F.R.C.P.(C)
La incidencia de cáncer anal es relativamente baja en la población general, pero es sustancialmente mayor en varios grupos de riesgo específicos. Estos incluyen individuos inmunodeprimidos debido a un trasplante de órganos sólidos, mujeres con antecedentes de cáncer relacionado con el VHP o precáncer de cuello uterino o vulva, y personas con VIH (PWH). Los hombres, las mujeres y las personas transgénero con VIH corren un riesgo sustancialmente mayor que la población general, y los hombres que tienen relaciones sexuales con hombres corren el mayor riesgo de todos. Además, todos los grupos en riesgo están en mayor riesgo con la edad avanzada, la duración de la infección o la inmunosupresión. Al igual que el cáncer cervical, el cáncer anal se asocia con el VPH, particularmente el VPH 16, y está precedido por una lesión precancerosa, lesión intraepitelial escamosa de alto grado (HSIL). El tratamiento del HSIL cervical es eficaz para reducir la incidencia del cáncer cervical, y forma la base para la prevención secundaria del cáncer cervical con cribado de HSIL cervical con citología y/o VPH, seguido de la colposcopia y el tratamiento del HSIL probado por biopsia.
Dada su alta incidencia de cáncer anal, y las similitudes entre el cáncer cervical y el cáncer anal, ha habido interés en la prevención secundaria del cáncer anal en los grupos de riesgo descritos anteriormente. Hasta hace poco no existían programas formales de cribado para el cáncer anal o HSIL, en gran parte debido a la ausencia de evidencia de que el tratamiento del HSIL sería efectivo para reducir el riesgo de progresión al cáncer anal. El estudio ANCHOR cambió eso, y mostró que el tratamiento del HSIL anal, principalmente con hifrecación basada en el consultorio (un procedimiento electroquirúrgico mínimamente invasivo, seguro y eficaz que utiliza una aguja pequeña y pulso eléctrico para realizar una ablación de lesiones sin cortar ni suturar), redujo la incidencia de cáncer anal en personas con VIH en un 57 % en comparación con personas cuyo HSIL no fue tratado. Con esta nueva información, la Sociedad Internacional de Neoplasia Anal publicó las pautas de cribado para grupos con mayor riesgo de cáncer anal, incluyendo aquellos con VIH. El 9 de julio de 2024, los Centros para el Control y la Prevención de Enfermedades de EE. UU., la HIV Medical Association y la Infectious Disease Society of America publicaron las primeras pautas federales para la prevención del cáncer anal en personas con VIH. Estas organizaciones recomiendan el cribado como estándar de atención para PWH (Figura 1,2), seguido de biopsia guiada por una anoscopia de alta resolución (HRA) de lesiones visibles, y la hifrecación como terapia de primera línea para el tratamiento del HSIL probado por biopsia (Figura 2).
Todavía queda mucho por aprender sobre los enfoques óptimos de cribado y el tratamiento optimizado del HSIL. Las pruebas de cribado actualmente recomendadas, citología y VPH, tienen limitaciones. La hifrecación en el estudio ANCHOR no evitó completamente la progresión de HSIL anal a cáncer anal. El Consorcio ULACnet CAMPO (Universidad de California, San Francisco, Universidad de Puerto Rico, Instituto Nacional de Salud Pública e Instituto de Cáncer Nacional) está a la vanguardia del tratamiento de estas cuestiones para las PWH latinoamericanas. Para posibilitar estos estudios, los equipos de los sitios de CAMPO en México y Puerto Rico fueron capacitados y certificados en HRA. ULACnet-101 está diseñado para optimizar los algoritmos de detección para hombres y mujeres con VIH mediante el examen de la realización de una variedad de pruebas para detectar HSIL anal y cáncer. Estos incluyen pruebas de VPH, citología, CINTEC-plus y metilación. El equipo de CAMPO también está abordando retos terapéuticos; ULACnet-102 estudiará la seguridad y eficacia de un probiótico para tratar el HSIL anal junto con los cambios asociados es el microbioma anal. ULACnet-103 evaluará diferentes programas de hifrecación como un medio para mejorar la eficacia de la hifrecación. En conjunto, estos estudios contribuirán a la implementación sostenible de estas nuevas pautas de estándar de atención para las PWH latinoamericanas. También apoyarán una sólida capacidad de investigación que contribuirá a la atención de las PWH latinoamericanas y de las poblaciones de PWH en todo el mundo.

Figura 1. Algoritmo de cribado del cáncer anal en personas asintomáticas con VIH [ 4 ]

Figura 2. Evaluación de los resultados de citología anal y VPH en personas con VIH [ 5 ]
Auditoria do Programa ULACNet: Um aspecto da garantia de qualidade

Eustaquia Chacon, Bacharel em Ciências
Gerente de Ensaios Clínicos
Membro da Diretoria do Programa de Pesquisa em Monitoramento Clínico
Laboratório Nacional Frederick para Pesquisa do Câncer
e
Christian Capriolo, Bacharel em Ciências
Associado de Pesquisa Clinica
Membro da Diretoria do Programa de Pesquisa em Monitoramento Clínico
Laboratório Nacional Frederick para Pesquisa do Câncer
Implementar um programa clínico envolve diversos processos, sendo que a garantia de qualidade é fundamental para assegurar a conformidade com padrões e diretrizes. No programa ULACNet, que se concentra em pesquisas clínicas apoiadas pelo Instituto Nacional do Câncer (NCI, na sigla em inglês), a auditoria desempenha um papel crucial na manutenção da integridade dos estudos e na conformidade regulatória. A auditoria é realizada em dois níveis no programa ULACNet: no nível da organização acadêmica líder (LAO, na sigla em inglês) e no nível da organização acadêmica (AO, na sigla em inglês). Este artigo é sobre o nível AO, também conhecido como auditoria de local.
Importância da Auditoria
A auditoria é fundamental no programa ULACNet para garantir a manutenção de altos padrões de pesquisa clínica e a conformidade com os rigorosos requisitos das concessões do NCI. Além da conformidade regulatória, o objetivo principal da auditoria é proteger o bem-estar dos participantes do estudo. Ao revisar sistematicamente os procedimentos do estudo, as auditorias verificam a conformidade com o protocolo e a implementação dos processos de qualidade descritos nas diretrizes do ULACNet. Este processo de revisão aumenta a credibilidade e a confiabilidade dos resultados do estudo.
O Processo de Auditoria
A auditoria dentro do programa ULACNet é um processo estruturado e meticuloso que envolve várias etapas principais:
1. Preparação
O processo de auditoria começa com o agendamento e a coordenação entre os auditores e os AOs responsáveis pela implementação dos protocolos de estudo. Os auditores confirmam a auditoria e, em seguida, revisam os protocolos do estudo, o plano de monitoramento e os relatórios de visita, relatórios de segurança e outros documentos relevantes. Enquanto isso, os AOs se preparam garantindo que todos os dados do estudo estejam completos, realizando verificações internas de qualidade e abordando quaisquer descobertas de auditoria anteriores ou problemas de conformidade. Esta fase inicial prepara o cenário para uma comunicação e colaboração eficazes entre auditores e AOs durante todo o processo de auditoria.
2. Visita de auditoria
As auditorias podem ser realizadas presencialmente ou remotamente, dependendo das considerações logísticas e das localizações geográficas dos locais de estudo dentro do programa ULACNet (incluindo países como Brasil, Peru, México, Haiti, República Dominicana e Estados Unidos). Durante uma visita de auditoria, os auditores revisam todos os aspectos do estudo de acordo com os requisitos do protocolo. Essa revisão inclui a verificação dos critérios de elegibilidade dos participantes, a adequação dos processos de consentimento informado, a confirmação de que todos os participantes assinaram o formulário de consentimento informado, o manuseio adequado de amostras para testes laboratoriais, a gestão de produtos investigacionais, a documentação de aprovações regulatórias e as qualificações e treinamento da equipe do estudo. Além disso, os auditores avaliam como os AOs comunicam desvios dos protocolos de estudo aprovados ou eventos inesperados que afetam a segurança dos participantes ou os objetivos do estudo.
3. Relatório de auditoria e acompanhamento
Após uma auditoria, um relatório é elaborado, descrevendo o status dos itens auditados e quaisquer discrepâncias ou áreas de melhoria identificadas. Se forem identificados problemas, eles serão comunicados ao AO por meio de uma carta de acompanhamento de auditoria detalhando o problema e sugerindo ações corretivas para abordar as descobertas. No programa ULACNet, o auditor geralmente acompanha as ações corretivas tomadas por um local para abordar as descobertas da auditoria, mas geralmente o associado de pesquisa clínica (CRA, na sigla em inglês) do local é responsável por garantir que as ações corretivas sejam implementadas. Por outro lado, se nenhum problema for encontrado, a carta de acompanhamento descreve as áreas auditadas e confirma a conclusão da auditoria sem preocupações significativas. Esses processos são essenciais para garantir transparência e responsabilidade, além de assegurar que o NCI DCP, patrocinador da concessão, esteja ciente da conformidade com os protocolos do estudo e os padrões regulatórios.
Desafios na auditoria do programa ULACNet
A auditoria apresenta desafios tanto para auditores quanto para os AOs envolvidos no programa ULACNet. Os auditores precisam lidar com contextos culturais e linguísticos diversos, especialmente em locais de estudo internacionais, onde as barreiras linguísticas podem complicar a comunicação e a compreensão das observações de auditoria. A maioria das auditorias no programa é realizada remotamente, o que apresenta desafios logísticos e pode dificultar as interações pessoais e a construção de relacionamento entre auditores e equipe do local de estudo, potencialmente afetando a clareza das descobertas da auditoria e a eficácia das ações corretivas.
Para os AOs, o processo de auditoria pode representar uma avaliação nova e rigorosa de suas práticas de pesquisa clínica, especialmente se elas não estiverem familiarizadas com os procedimentos de auditoria ou tiverem experiência limitada com inspeções regulatórias. Isso exige uma preparação e coordenação minuciosas para garantir que toda a documentação e os processos relacionados ao estudo sejam revisados e estejam em conformidade com as diretrizes do ULACNet e do NCI.
Perspectiva profissional
Do ponto de vista do auditor, participar das auditorias do ULACNet representa uma conquista profissional significativa. Garantir a integridade e a qualidade dos ensaios clínicos não apenas mantém os padrões éticos, mas também contribui para o avanço da pesquisa médica e para a melhoria dos resultados dos cuidados de saúde, especialmente em comunidades hispânicas carentes. Os auditores devem contribuir para construir uma base sólida de confiança e credibilidade na pesquisa clínica, o que é essencial para promover colaborações entre pesquisadores, instituições e participantes do estudo.
Conclusão
A auditoria dentro do programa ULACNet é essencial para manter os mais altos padrões de pesquisa clínica e conformidade regulatória. Ao revisar sistematicamente protocolos, procedimentos e dados do estudo, as auditorias garantem que a pesquisa conduzida sob o programa ULACNet esteja em conformidade com os padrões estabelecidos pelo NCI e outros órgãos reguladores. À medida que a pesquisa clínica evolui, o papel da auditoria continua sendo fundamental para proteger o bem-estar dos participantes, garantir a integridade dos dados e validar os resultados do estudo. Por meio de práticas de auditoria eficazes, os stakeholders do programa ULACNet podem garantir seu compromisso com a excelência em pesquisa clínica e contribuir de forma significativa para o avanço do conhecimento científico e da inovação em saúde.
Legendas de figuras
Bem-vindo ao ULACNet Update , onde compartilhamos atualizações programáticas e de pesquisa para a US-Latin American-Caribbean HIV/HPV-Cancer Prevention Clinical Trials Network (ULACNet)!
Sur cette page
- Vivre avec le VIH et prévenir le cancer du col de l'utérus: Lancement d'une étude transformatrice - ULACNet 202
- Analyse AQuIP: Évaluation de l'inscription des patients aux études de dépistage ULACNet
- Dépistage et prévention du cancer de l'anus en tant que norme de soins pour les personnes atteintes du VIH : les nouvelles lignes directrices
- Audit du programme ULACNet : Un aspect de l’assurance qualité
Vivre avec le VIH et prévenir le cancer du col de l'utérus: Lancement d'une étude transformatrice - ULACNet 202
(Consortium ROCCHHA - Site du Mexique)
Par: Alejandra Portillo-Romero, M.D, Sc.D., Betania Allen-Leigh, Ph.D., Eduardo Lazcano-Ponce, MD, Sc.D., Instituto Nacional de Salud Pública (INSP)
Le recrutement de femmes vivant avec le VIH (WLHIV) pour des projets de recherche axés sur la prévention du cancer du col de l'utérus est une tâche cruciale et multiforme qui nécessite une approche stratégique et sensible. Les femmes vivant avec le VIH courent un risque nettement plus élevé de développer un cancer du col de l'utérus en raison de la prévalence accrue des infections persistantes par le virus du papillome humain (HPV). Ces infections, si elles ne sont pas détectées et traitées à temps, peuvent évoluer vers des lésions malpighiennes intra-épithéliales de haut grade (HSIL) et finalement vers un cancer invasif du col de l'utérus. L'étude intitulée "Optimisation du dépistage du cancer du col de l'utérus chez les femmes vivant avec le VIH dans les pays d'Amérique latine" vise à mettre au point un test HPV à haut risque et un test moléculaire au point d'intervention qui optimisent la spécificité de la détection des lésions malpighiennes intraépithéliales de haut grade (CIN2+) chez les WLHIV tout en maintenant une sensibilité élevée du test.
Le recrutement des WLHIV dans des études de recherche présente de nombreux défis, notamment la stigmatisation associée au VIH, le manque d'informations, l'acceptation et la participation limitées des prestataires de soins de santé, ainsi que les obstacles logistiques et financiers (Figure 1).
Figure 1. Obstacles au dépistage du papillome humain (HPV) [ 1 ]

Conférence "L’éradication du cancer du col de l'utérus : Le cas du Mexique", par Dr Eduardo Lazcano
Il est essentiel de mettre en œuvre des stratégies de recrutement qui s'attaquent à ces obstacles. Sur le site du Mexique au sein du ROCCHHA, nous avons abordé certains obstacles comme suit:
1. Collaboration et intégration avec le personnel de la clinique VIH (CAPASITS Puebla) et de l'hôpital pour femmes de Puebla
Nous avons impliqué le personnel dirigeant et opérationnel de la clinique et de l'hôpital pour faciliter la mise en œuvre de l'étude dans l'unité de dysplasie de l'hôpital pour femmes. Nous avons organisé une présentation du projet à l'hôpital, en soulignant son importance, ses objectifs et ses avantages pour les WLHIV. Au cours de cette présentation, le Dr Eduardo Lazcano a donné une conférence sur "L'éradication du cancer du col de l'utérus : Le cas du Mexique", à laquelle ont assisté les directeurs, les médecins de l'hôpital, les résidents en gynécologie, les étudiants en médecine et les membres de l'équipe de l'INSP.
2. Education et sensibilisation des femmes fréquentant la clinique VIH
Les médecins de la clinique VIH s'efforcent de fournir à leurs patientes vivant avec le VIH des informations claires et accessibles sur les avantages du dépistage du cancer du col de l'utérus, en saisissant toutes les occasions lors des consultations médicales, des rendez-vous de vaccination, de l'administration de la thérapie antirétrovirale (ART) et des visites de laboratoire clinique. En outre, une infirmière qualifiée organise des séances d'information à l'intention des utilisateurs de soins de santé, expliquant la relation entre le papillome humain et le cancer du col de l'utérus, afin de promouvoir une participation active aux programmes de santé préventive et d'encourager l'implication dans l'étude.

Dysplasies Zone où sont réalisées les colposcopies. Hôpital pour femmes, Puebla, Mexique
3. Adéquation des espaces et approvisionnement en fournitures médicales
La capacité limitée des systèmes de santé dans les pays à revenus moyens et faibles peut entraîner des retards dans le diagnostic et le traitement des lésions précancéreuses. Nous visons à optimiser le processus de prise en charge de la dysplasie afin d'éviter que les participantes à notre étude ne soient soumises à des procédures administratives complexes pour obtenir une colposcopie et de s'assurer qu'elles reçoivent un traitement dans un délai court, minimisant ainsi la perte de suivi. En outre, nous fournissons à l'hôpital pour femmes de Puebla le matériel médical nécessaire (qui fait souvent défaut) pour offrir des soins médicaux de meilleure qualité, ce qui permet aux colposcopistes de s'occuper d'un plus grand nombre de femmes (et pas seulement des participantes à l'étude).
4. Atténuer la stigmatisation et la peur de la discrimination chez les participants

Katia Cruz-González (coordinatrice du site) a mené le processus de consentement éclairé, expliquant en détail aux participants les mesures de confidentialité entourant leurs données
Il est essentiel de garantir la confidentialité des données des participants et d'adopter une approche sensible et respectueuse de leurs besoins et préoccupations. C'est pourquoi le personnel de la clinique VIH, de l'hôpital pour femmes de Puebla et de l'INSP est continuellement formé à traiter les personnes vivant avec le VIH avec dignité et respect. L'objectif est d'éviter que les femmes ne se sentent jugées ou maltraitées, afin qu'elles ne manquent pas l'occasion d'être dépistées et traitées à temps si nécessaire. Une fois que les femmes sont inscrites à l'étude, elles reçoivent des informations claires et précises sur la protection de leurs données personnelles, et le personnel maintient une communication constante jusqu'à ce qu'elles reçoivent leurs résultats.
5. Formation continue des professionnels de la santé
À l'INSP, nous nous sommes toujours engagés à assurer la formation continue des professionnels de la santé. Grâce à la collaboration avec l'Hôpital des femmes de Puebla, nous visons à impliquer les résidents en gynécologie ainsi que les gynécologues et colposcopistes plus expérimentés dans la formation et la recherche, en encourageant l'amélioration des pratiques de dépistage et le traitement des lésions précancéreuses. Par exemple, en juillet 2024, les membres de notre équipe donneront un cours en ligne sur la recherche en santé publique aux résidents en gynécologie de l'hôpital pour femmes de Puebla.
Enfin, la participation à cet essai ne profite pas seulement aux participants en leur donnant accès à des interventions préventives et à un suivi médical continu, mais génère également des connaissances précieuses qui peuvent influencer les politiques de santé publique et améliorer les programmes de prévention du cancer du col de l'utérus dans notre pays, le Mexique.
Analyse AQuIP: Évaluation de l'inscription des patients aux études de dépistage ULACNet
Par Amina Chtourou, M.P.H.
Dans le but de promouvoir l'efficacité des essais cliniques et d'améliorer le recrutement et la rétention des participants, le programme d'amélioration de la qualité des essais (AQuIP) a été mis en place comme outil de suivi des essais cliniques dans toutes les études du réseau d'essais cliniques de prévention du VIH/HPV-cancer des États-Unis, de l'Amérique latine et des Caraïbes (US-Latin American-Caribbean HIV/HPV-Cancer Prevention Clinical Trials Network - ULACNet). Le programme AQuIP a été développé par Ellen Richmond, M.S., GNP-BC à la Division de prévention du cancer (DCP) de l'Institut national du cancer et a été utilisé dans plusieurs réseaux d'essais cliniques de prévention du cancer de la DCP, y compris ULACNet, au cours des dix dernières années. L'AQuIP fournit une plateforme permettant au personnel de recherche de collecter et de saisir les données relatives aux participants à travers les différentes étapes du processus de recrutement des essais cliniques, y compris le nombre de participants potentiels sélectionnés, les stratégies de recrutement utilisées, le nombre de participants ayant donné leur accord et les raisons pour lesquelles ils n'ont pas donné leur accord ou n'ont pas participé à l'intervention. En outre, l'AQuIP utilise un journal d'étude pour permettre au personnel de recherche de documenter les événements à l'échelle de l'étude et du site qui peuvent avoir un impact positif ou négatif sur le recrutement. Les exemples d'entrées dans le journal peuvent inclure des changements dans le nombre de membres du personnel du site (perte de personnel ou nouvelles embauches), des retards dans la réception des agents ou des fournitures de l'étude, des problèmes liés aux conditions météorologiques (par exemple, un ouragan), etc. Par conséquent, l'AQuIP permet d'identifier les éventuels obstacles au recrutement des participants et de modifier le protocole afin d'atteindre plus rapidement le nombre d'inscriptions prévu.
Les données de l'AQuIP sont soumises à la DCP sur une base mensuelle. Nous avons analysé les données de l'AQuIP pour trois études de dépistage ULACNet (ULACNet-101, ULACNet-202 et ULACNet-302), depuis le début du recrutement des patients en novembre 2021 jusqu'en mai 2024, afin de comprendre comment les différentes études ont mis en œuvre l'utilisation de l'AQuIP, d'évaluer le recrutement des participants dans les études ULACNet et d'évaluer l'applicabilité de l'AQuIP dans les essais cliniques en dehors des milieux américains. À ce jour, dans les trois
études de sélection, 1 988 personnes ont signé le consentement et 1 965 ont commencé l'intervention de l'étude, comme le montre le tableau 1.
| Numéro de l'étude | Nombre de consentements signés | Nombre de personnes ayant commencé l'intervention de l'étude | Inscriptions ciblées | Statut de l'étude |
|---|---|---|---|---|
| ULACNet-101 | 1,107 | 1,106 | 1,500 | en cours |
| ULACNet-202 | 252 | 251 | 1,000 | en cours |
| ULACNet-302 | 629 | 608 | 600 | Inscriptions terminées |
| Total | 1,988 | 1,965 | 3,100 |
Les stratégies de recrutement les plus courantes dans les trois études de dépistage étaient les stratégies "autres", les recommandations des médecins et les recommandations par le personnel de l'établissement qui ne faisait pas partie du personnel de l'étude. La figure 1 ci-dessous montre les stratégies de recrutement employées dans les trois études de dépistage. En ce qui concerne les "raisons de ne pas consentir", le personnel de l'étude a souvent fait état d'une "autre" raison, d'un refus de la part de la personne ou d'un antécédent de cancer. La figure 2 ci-dessous présente les "raisons de ne pas consentir" dans les trois études de dépistage. La figure 2 se limite aux personnes qui ont été contactées mais qui n'ont pas consenti à participer à l'étude et ne reflète pas nécessairement les raisons pour lesquelles les participants n'ont pas pu commencer l'intervention de l'étude après avoir signé le formulaire de consentement.

Figure 1. Études de sélection ULACNet - Stratégies de recrutement des participants [ 2 ]

Figure 2. Études de sélection ULACNet - Raisons pour lesquelles les personnes n'ont pas signé le consentement [ 3 ]
Après avoir analysé les stratégies de recrutement et les motifs de refus, nous avons constaté que l'AQuIP devrait être amélioré pour mieux répondre aux besoins des sites internationaux, car certaines stratégies de recrutement et certains motifs de refus des participants ne sont pas toujours applicables dans les pays autres que les États-Unis (É.-U.). Par exemple, les stratégies de recrutement incluent le service postal américain comme option, et les raisons pour lesquelles les participants n'ont pas donné leur consentement incluent des options telles que Snowbird (ceux qui, aux États-Unis, se rendent dans des climats plus chauds pendant les mois d'hiver). Le personnel d'étude des autres pays pourrait également bénéficier d'une formation à la saisie des données de l'AQuIP et d'instructions et de définitions améliorées sur les sélections de l'AQuIP afin de catégoriser avec plus de précision les stratégies de recrutement et les raisons du non-consentement. Actuellement, le personnel de l'étude identifie les raisons pour lesquelles un participant n'est pas éligible dans la colonne "raisons de ne pas consentir" ; nous recommandons donc d'ajouter une nouvelle colonne pour identifier spécifiquement la ou les raisons de l'inéligibilité.
Les données de l'AQuIP peuvent également être combinées avec d'autres sources de données pour évaluer les événements indésirables par participant signalés pour chaque protocole et examiner les données démographiques, telles que le genre, l'âge et la race, des participants qui ont consenti à participer à l'étude. Dans l'ensemble, s'il est correctement mis en œuvre sur les sites d'étude, le système AQuIP fournit une mine d'informations sur le recrutement, les inscriptions, les difficultés et les réussites au niveau de l'individu, du site, du protocole et du réseau. Nous pouvons continuer à utiliser et à adapter l'AQuIP afin d'améliorer la conception des études cliniques et de maximiser l'efficacité du recrutement des participants.
A propos de l'auteur

Je m'appelle Amina Chtourou et je suis Presidential Management Fellow (PMF) à l'Institut national du cancer des États-Unis (NCI). Avant de commencer le programme PMF, j'ai obtenu un M.P.H. en épidémiologie à l'université de Pittsburgh et j'ai travaillé au service de santé du comté d'Allegheny sur la surveillance des overdoses. En tant que PMF affecté au NCI, j'ai eu l'occasion d'effectuer quatre rotations au sein de l'institut et une mission de développement à l'Agence américaine pour le développement international (USAID) au cours des deux dernières années. Au NCI, j'ai effectué des rotations au sein du programme de recherche sur la surveillance de la division de la lutte contre le cancer et des sciences de la population, au bureau des relations avec le Gouvernement et le Congrès, au Centre pour la santé mondiale, et ici, à la DCP. À l'USAID, j'ai travaillé au Bureau de la santé mondiale, au Bureau du VIH/sida, à la Division de l'information stratégique, de l'évaluation et de l'informatique, où je soutenais l'équipe technique chargée du cancer du col de l'utérus en tant qu'analyste de données et agent de liaison pour l'information stratégique (IS). J'ai également participé à la planification opérationnelle régionale du PEPFAR pour la région de l'hémisphère occidental, qui comprend les Caraïbes, l'Amérique centrale et l'Amérique du Sud.
J'ai décidé d'effectuer ma dernière rotation PMF ici à la DCP pour continuer à apprendre sur les cancers liés au HPV, découvrir le rôle d'agent de programme (PO) ici au NIH, et ce à quoi ressemblent les scientifiques de projet et d'autres membres clés du personnel pour soutenir les accords coopératifs/réseaux d'essais cliniques. Au cours de ma rotation au sein de la DCP, j'ai eu l'occasion de me familiariser avec le processus du cycle de financement des subventions et d'examiner les rapports d'avancement de la recherche (RPPR) soumis par les chercheurs principaux (PI) des réseaux ULACNet et CASCADE. J'ai également réalisé une analyse à l'aide du programme d'amélioration de la qualité de l'accumulation, AQuIP, que la DCP a mis en place en tant que programme de contrôle de l'accumulation pour ULACNet.
Après mon passage à la DCP, j'occuperai un poste permanent au Centre pour la santé mondiale du NCI. Je suis ravie de continuer à développer mes compétences en matière de santé mondiale et de contribuer à la recherche et à la lutte contre le cancer dans le monde. J'ai hâte de collaborer avec mes collègues de la DCP à l'avenir et de continuer à m'informer sur le travail extraordinaire réalisé par ULACNet et CASCADE.
Dépistage et prévention du cancer de l'anus en tant que norme de soins pour les personnes atteintes du VIH : les nouvelles lignes directrices
Par: Joel Palefsky, M.D., C.M., F.R.C.P.(C)
L'incidence du cancer de l'anus est relativement faible dans la population générale, mais elle est nettement plus élevée dans plusieurs groupes à risque spécifiques. Il s'agit notamment des personnes immunodéprimées à la suite d'une transplantation d'organe solide, des femmes ayant des antécédents de cancer ou de pré-cancer du col de l'utérus ou de la vulve liés au papillomavirus (VPH) et des personnes séropositives. Les hommes, les femmes et les transsexuels séropositifs courent tous un risque nettement plus élevé que la population générale, les hommes ayant des rapports sexuels avec d'autres hommes étant les plus exposés. En outre, tous les groupes à risque sont plus exposés en raison de l'âge, de la durée de l'infection ou de l'immunosuppression. Comme le cancer du col de l'utérus, le cancer de l'anus est associé au VPH, en particulier au VPH 16, et est précédé d'une lésion précancéreuse, la lésion malpighienne intraépithéliale de haut grade (HSIL). Le traitement de la HSIL cervicale est efficace pour réduire l'incidence du cancer du col de l'utérus et constitue la base de la prévention secondaire du cancer du col de l'utérus par le dépistage de la HSIL cervicale par cytologie et/ou HPV, suivi d'une colposcopie et d'un traitement de la HSIL prouvée par biopsie.
Compte tenu de l'incidence élevée du cancer de l'anus et des similitudes entre le cancer du col de l'utérus et le cancer de l'anus, la prévention secondaire du cancer de l'anus dans les groupes à risque décrits ci-dessus a suscité de l'intérêt. Jusqu'à récemment, il n'existait pas de programme officiel de dépistage du cancer de l'anus ou de la HSIL, principalement en raison de l'absence de preuves de l'efficacité du traitement de la HSIL pour réduire le risque d'évolution vers un cancer de l'anus. L'étude ANCHOR a changé la donne et a montré que le traitement de la HSIL anale, principalement par hyfrecation en cabinet (une procédure électro-chirurgicale peu invasive, sûre et efficace qui utilise une petite aiguille et une impulsion électrique pour ablater les lésions sans couper ni suturer), réduisait de 57 % l'incidence du cancer de l'anus chez les personnes séropositives par rapport aux personnes dont la HSIL n'avait pas été traitée. Forte de ces nouvelles informations, la Société internationale de néoplasie anale a publié des directives de dépistage pour les groupes présentant un risque accru de cancer anal, y compris les personnes séropositives. Le 9 juillet 2024, les Centres américains de contrôle et de prévention des maladies, l'Association médicale du VIH et la Société des maladies infectieuses d'Amérique ont publié les premières lignes directrices fédérales pour la prévention du cancer de l'anus chez les personnes séropositives. Ces organisations recommandent le dépistage comme norme de soins chez les PWH (Figure 1,2), suivi d'une biopsie guidée par anoscopie à haute résolution (HRA) des lésions visibles, et l'hyfrécation comme traitement de première intention pour le traitement des HSIL prouvées par biopsie (Figure 2).
Il reste encore beaucoup à apprendre sur les approches optimales de dépistage et de traitement de la HSIL. Les tests de dépistage actuellement recommandés, la cytologie et le VPH, présentent tous deux des limites. Dans l'étude ANCHOR, l'hyfrécation n'a pas complètement empêché la progression de la HSIL anale vers le cancer de l'anus. Le consortium ULACNet CAMPO (Université de Californie, San Francisco, Université de Porto Rico, Instituto Nacional de Salud Publica et Instituto de Cancer Nacional) est à l'avant-garde de l'étude de ces questions dans la santé publique latino-américaine. Pour permettre la réalisation de ces études, les équipes des sites CAMPO du Mexique et de Porto Rico ont été formées et certifiées en HRA. ULACNet-101 est conçu pour optimiser les algorithmes de dépistage pour les hommes et les femmes séropositifs en examinant les performances d'une variété de tests pour détecter la HSIL et le cancer de l'anus. Il s'agit notamment du test HPV, de la cytologie, de CINTec-PLUS et de la méthylation. L'équipe CAMPO aborde également des défis thérapeutiques; ULACNet-102 étudiera la sécurité et l'efficacité d'un probiotique pour traiter la HSIL anale ainsi que les changements associés dans le microbiome anal. ULACNet-103 évaluera différents calendriers d'hyfrécation comme moyen d'améliorer l'efficacité de l'hyfrécation. L'ensemble de ces études contribuera à la mise en œuvre durable de ces nouvelles directives de soins standard dans les PWH d'Amérique latine. Elles soutiendront également une solide capacité de recherche qui contribuera aux soins des PWH d'Amérique latine et des populations de PWH du monde entier.

Figure 1. Algorithme de dépistage du cancer de l'anus chez les personnes séropositives asymptomatiques [ 4 ]

Figure 2. Évaluation des résultats de la cytologie anale et du VPH chez les personnes séropositives [ 5 ]
Audit du programme ULACNet : Un aspect de l’assurance qualité

Par Eustaquia Chacon, B.S.
Gestionnaire des essais cliniques
Direction du programme de recherche sur la surveillance clinique
Laboratoire national de recherche sur le cancer de Frederick
et
Christian Capriolo, B.S.
Associé de recherche clinique
Direction du programme de recherche sur la surveillance clinique
Laboratoire national de recherche sur le cancer de Frederick
La mise en œuvre d'un programme clinique implique de nombreux processus, avec une assurance qualité essentielle pour garantir le respect des normes et des lignes directrices. Dans le cadre du programme ULACNet, qui se concentre sur la recherche clinique soutenue par l'Institut national du cancer (NCI), l'audit joue un rôle crucial dans le maintien de l'intégrité de l'étude et de la conformité réglementaire. L'audit est réalisé à deux niveaux dans le programme ULACNet : au niveau de l'organisation universitaire principale (LAO) et au niveau de l'organisation universitaire (AO). Cet article se concentre sur le niveau AO, également connu sous le nom d'audit de site.
Importance de l’audit
L'audit est essentiel dans le programme ULACNet pour respecter les normes rigoureuses de la recherche clinique et répondre aux exigences strictes de la subvention du NCI. Au-delà de la conformité réglementaire, l'objectif premier de l'audit est de protéger le bien-être des participants à l'étude. En examinant systématiquement les procédures de l'étude, les audits vérifient le respect du protocole et la mise en œuvre des processus de qualité décrits dans les lignes directrices d'ULACNet. Ce processus d'examen renforce la crédibilité et la fiabilité des résultats de l'étude.
Le processus d’audit
L'audit dans le cadre du programme ULACNet est un processus structuré et méticuleux qui comporte plusieurs étapes clés
1. Préparation
Le processus d'audit commence par la programmation et la coordination entre les auditeurs et les AO responsables de la mise en œuvre des protocoles d'étude. Les auditeurs confirment l'audit, puis examinent les protocoles d'étude, le plan de surveillance et les rapports de visite, les rapports de sécurité et d'autres documents pertinents. Pendant ce temps, les AO se préparent en s'assurant que toutes les données de l'étude sont complètes, en effectuant des contrôles de qualité internes et en abordant toute constatation d'audit antérieure ou tout problème de conformité. Cette phase initiale prépare le terrain pour une communication et une collaboration efficaces entre les auditeurs et les AO tout au long du processus d'audit.
2. Visite d'audit
Les audits peuvent être réalisés sur place ou à distance, en fonction de considérations logistiques et de la situation géographique des sites d'étude dans le cadre du programme ULACNet (y compris des pays comme le Brésil, le Pérou, le Mexique, Haïti, la République dominicaine et les États-Unis). Lors d'une visite d'audit, les auditeurs examinent tous les aspects de l'étude conformément aux exigences du protocole. Ils vérifient notamment les critères d'éligibilité des participants, l'adéquation des procédures de consentement éclairé, la signature d'un formulaire de consentement éclairé par tous les participants à l'étude, la manipulation correcte des échantillons pour les tests de laboratoire, la gestion des produits expérimentaux, la documentation des approbations réglementaires, ainsi que les qualifications et la formation du personnel de l'étude. En outre, les auditeurs évaluent la manière dont les AO communiquent les écarts par rapport aux protocoles d'étude approuvés ou les événements inattendus affectant la sécurité des participants ou les objectifs de l'étude.
3. Rapport d'audit et suivi
Après un audit, un rapport est rédigé, décrivant l'état d'avancement des éléments audités et les éventuelles divergences ou domaines d'amélioration identifiés. Si des problèmes sont identifiés, ils sont communiqués à l'AO via une lettre de suivi de l'audit détaillant le problème et suggérant des actions correctives pour répondre aux constatations. Dans le cadre du programme ULACNet, l'auditeur assure généralement le suivi des mesures correctives prises par un site pour répondre aux conclusions de l'audit, mais c'est généralement l'attaché de recherche clinique (ARC) du site qui est chargé de veiller à ce que les mesures correctives soient mises en œuvre. Inversement, si aucun problème n'est constaté, la lettre de suivi décrit les domaines audités et confirme que l'audit a été mené à bien sans problème majeur. Ces processus sont essentiels pour assurer la transparence et la responsabilité, et pour garantir que le NCI DCP, le commanditaire de la subvention, est informé du respect des protocoles d'étude et des normes réglementaires.
Défis liés à l'audit du programme ULACNet
L'audit présente des défis tant pour les auditeurs que pour les AO participant au programme ULACNet. Les auditeurs doivent naviguer dans divers contextes culturels et linguistiques, en particulier sur les sites d'étude internationaux où les barrières linguistiques peuvent compliquer la communication et la compréhension des observations d'audit. La plupart des audits du programme sont effectués à distance, ce qui pose des problèmes logistiques et peut entraver les interactions personnelles et l'établissement de rapports entre les auditeurs et le personnel du site, ce qui peut affecter la clarté des conclusions de l'audit et l'efficacité des mesures correctives.
Pour les AO, le processus d'audit peut représenter une évaluation nouvelle et rigoureuse de leurs pratiques de recherche clinique, en particulier si elles ne sont pas familiarisées avec les procédures d'audit ou si elles ont une expérience limitée des inspections réglementaires. Cela nécessite une préparation et une coordination approfondies pour s'assurer que tous les documents et processus liés à l'étude sont examinés et conformes aux lignes directrices d'ULACNet et du NCI.
Perspective professionnelle
Du point de vue d'un auditeur, la participation aux audits ULACNet représente un accomplissement professionnel important. Garantir l'intégrité et la qualité des essais cliniques permet non seulement de respecter les normes éthiques, mais aussi de faire progresser la recherche médicale et d'améliorer les résultats des soins de santé, en particulier au sein des communautés hispaniques mal desservies. Les auditeurs devraient contribuer à établir une base solide de confiance et de crédibilité dans la recherche clinique, ce qui est essentiel pour favoriser les collaborations entre les chercheurs, les institutions et les participants aux études.
Conclusion
L'audit au sein du programme ULACNet fait partie intégrante du maintien des normes les plus élevées en matière de recherche clinique et de conformité réglementaire. En examinant systématiquement les protocoles, les procédures et les données de l'étude, les audits garantissent que la recherche menée dans le cadre du programme ULACNet respecte les normes établies par le NCI et d'autres organismes de réglementation. Au fur et à mesure que la recherche clinique évolue, le rôle de l'audit reste essentiel pour préserver le bien-être des participants, garantir l'intégrité des données et valider les résultats de l'étude. Grâce à des pratiques d'audit efficaces, les parties prenantes du programme ULACNet peuvent en toute confiance respecter leur engagement en faveur de l'excellence dans la recherche clinique et contribuer de manière significative à l'avancement des connaissances scientifiques et à l'innovation dans le domaine des soins de santé.
Légendes des figures
Subscribe to ULACNet Update. For more information on ULACNet, please contact ULACNet@mail.nih.gov.
